Диссоциация - сильный электролит
Cтраница 3
Величина / рассматривается как кажущаяся степень диссоциации сильных электролитов. Она отражает все имеющие место в данной системе взаимодействия силовых полей. [31]
 |
Ионная оболочка вокруг катиона ( а и со - а С. [32] |
Вследствие образования ионной атмосферы к процессу диссоциации сильных электролитов нельзя применять закон действия масс, так как в выражение константы равновесия входят концентрации свободных ионов, которых в реальных растворах нет. [33]
Величина / рассматривается как кажущаяся степень диссоциации сильных электролитов. Она отражает все имеющие место в данной системе взаимодействия силовых полей. [34]
Примем, что концентрации ионов определяются диссоциацией сильных электролитов и потому пренебрежем тем количеством ионов, которое дает слабо диссоциирующая кислота НА. [35]
Величину у часто рассматривают как кажущуюся степень диссоциации сильных электролитов. [36]
Величину f часто рассматривают как кажущуюся степень диссоциации сильных электролитов. Активность ионов, так же как и концентрация, выражается в s - ион / л и является как бы их эффективной концентрацией. [37]
В заключение отметим, что определение констант диссоциации сильных электролитов является далеко не тривиальным делом и требует строгого соблюдения ряда экспериментальных условий, а также максимально достижимой точности аналитических методов определения концентраций распределяемого электролита в каждой из фаз. [38]
VII были рассмотрены новейшие методы вычисления констант диссоциации сильных электролитов в средах с низкой диэлектрической постоянной и слабых электролитов и водных растворах из данных по электропроводности. Константы диссоциации, полученные из этих данных, в большинство случаев определены точно только для 25, и поэтому их нельзя использовать для вычисления тсплот диссоциации и других термодинамических величин, слизанных с реакциями диссоциации. [39]
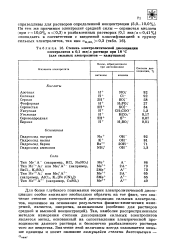
Как видно из приведенных данных, константа диссоциации сильных электролитов увеличивается с ростом концентрации. [40]
 |
Степень электролитической диссоциации. [41] |
Так, наиболее распространенным методом измерения степени диссоциации сильных электролитов является метод, основанный на сопоставлении электрической проводимости данного раствора и бесконечно разбавленного раствора того же вещества. [42]
Чем объясняются пониженные значения экспериментально определяемой степени диссоциации сильных электролитов по сравнению с действительной. Почему это расхождение уменьшается при разбавлении растворов. [43]
В заключение отметим, что определение констант диссоциации сильных электролитов является далеко не тривиальным делом и требует строгого соблюдения ряда экспериментальных условий, а также максимально достижимой точности аналитических методов определения концентраций распределяемого электролита в каждой из фаз. [44]
 |
Степень электролитической диссоциации. [45] |
Страницы: 1 2 3 4