Дальнейшая диссоциация
Cтраница 1
Дальнейшая диссоциация практически не увеличивает кислотности раствора. Хотя реакция нейтрализации сравнительно концентрированных растворов кислоты щелочью по первой ступени протекает количественно, на кривой кондуктометриче-ского титрования не имеется излома, соответствующего нейтрализации первого кислотного эквивалента. Это объясняется тем, что подвижности ионов Н2АзОз и НАзОз мало различаются, и электропроводность продолжает увеличиваться. Так как реакция нейтрализации второго кислотного эквивалента сильно обратима, значительное увеличение электропроводности раствора вследствие накопления в растворе гидроксильных ионов происходит после первой ступени нейтрализации. Таким образом, кондуктометриче-ское определение мышьяковистой кислоты в водных растворах невозможно, так как кривая титрования не имеет изломов. [1]
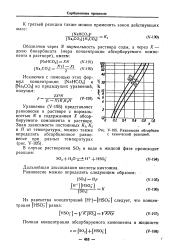 |
Равновесие абсорбции с химической реакцией. [2] |
Дальнейшая диссоциация кислоты ничтожна. [3]
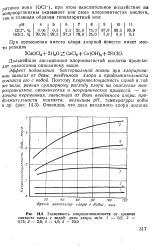 |
Зависимость хлоропоглощаемостн от времени контакта хлора с водой. дозы хлора, мг / л. 1 - 0 5. 2 - 0 75. 3 - 2 0. 4 - 4 0. 5 - 20 0. [4] |
Дальнейшая диссоциация хлорноватистой кислоты происходит аналогично описанному выше. [5]
Дальнейшая диссоциация галидов ЭГ на атомы требует затраты около 130 ( F) или 100 ( С1); ккал / моль. [6]
При дальнейшей диссоциации отщепляется еще один протон, а второй переходит к азоту. По Чепмэну, существование двойного бетаина неправдоподобно вследствие взаимного отталкивания. [7]
При дальнейшей диссоциации сульфата и увеличении содержания СаО в материале от 88 до 96 % температура плавления повышается с 1380 до 1480 С. Интересно отметить, что чистая окись кальция, по литературным данным [2], плавится при 2572 С. [8]
Может происходить и дальнейшая диссоциация комплексного иона на его компоненты, хотя и в очень слабой степени. [9]
Это приводит к дальнейшей диссоциации окрашенного комплекса, в результате чего комплекс разрушается. [10]
К - При повышенных температурах происходит дальнейшая диссоциация CF. CF [24], но C2F2 не был обнаружен в исследованном диапазоне температур. [11]
Ионы HS -, конечно, подвергаются дальнейшей диссоциации. [12]
Выделение на катоде ионов Н 1 вызывает дальнейшую диссоциацию воды на ионы Н и ОНГ, При этом ионы гидроксила взаимодействуют остающимися в растворе ионами Na, образуя едкий натр. [13]
 |
Относительные интенсивности главных линий масс-спектров эфиров. [14] |
Это показывает, что молекулярный ион сразу претерпевает дальнейшую диссоциацию. [15]
Страницы: 1 2 3 4