Электролитическая диссоциация - вода
Cтраница 2
Величина ионного произведения воды возрастает с повышением температуры, так как при этом увеличивается степень электролитической диссоциации воды и возрастают концентрации ионов гидроксония и гидроксид-ионов. [16]
Электрохимическое оксидирование ( анодирование) происходит за счет кислорода, выделяющегося около обрабатываемой анодной поверхности при электролитической диссоциации воды. На анодируемой поверхности алюминия в начале процесса образуется тонкая ( 0 01 - 0 1 мк) сплошная пленка окиси. [17]
Отсюда следует, что процесс ( 3) может конкурировать с процессом ( 2), что проявляется в частичной электролитической диссоциации воды. [18]
ОН -: Отсюда следует, что процесс ( 3) может конкурировать с процессом ( 2), что проявляется в частичной электролитической диссоциации воды. [19]
Справедливы ли эти определения применительно к неводным растворам, где не может быть и речи о существовании ионов водорода и гидроксил-ионов, образующихся за счет электролитической диссоциации воды. Какие вещества называют кислотами и основаниями, когда речь идет о неводных растворах. [20]
Оек хотя и зависят от концентрации ОН и Н ионов, но это влияние не сказывается на их разности, так как концентрации Н и ОН связаны равновесием электролитической диссоциации воды. Однако, как только ток начинает проходить сквозь ванну, на электродах устанавливается уже не равновесный потенциал, а на каждом электроде появляется еще напряжение поляризации, затрудняющее прохождение тока. [21]
В настоящее время доказано, что, помимо воды, существует много других неорганических и органических растворителей, которые в результате диссоциаций также образуют ионы, аналогичные по своей природе ионам, образующимся при электролитической диссоциации воды. [22]
При смешении эквивалентных количеств слабой кислоты и сильного основания остается некоторое количество нейтральных молекул кислоты и соответствующее, количество ионов ОН ( активного, действующего на лакмус основания), соотношение которых регулируется постоянными электролитической диссоциации воды и кислоты. Раствор поэтому имеет щелочную реакцию. [23]
Таким образом, гидролизом в широком смысле слова называют реакции взаимодействия различных веществ ( солей, гидридов, оксисоеди-нений, галоген -, тио - и цианангидридов) с ионами воды, сопровождающиеся нарушением равновесия электролитической диссоциации воды и изменением рН раствора. [24]
Таким образом, гидролизом в широком смысле слова называют реакции взаимодействия различных веществ ( солей, гидридов, оксисоединений, галоген -, тио - и цианангидридов) с ионами воды, сопровождающиеся нарушением равновесия электролитической диссоциации воды и изменением рН раствора. [25]
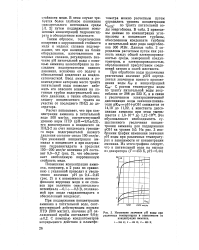 |
Изменение значения рН воды при. [26] |
При обработке воды щелочными реагентами значение рОН определяется значением ионного произведения воды Kvf и концентрацией Сон - С ростом температуры воды по тракту питательной воды энергоблока от 298 до 523 К, и в связи с увеличением электролитической диссоциации воды значение показателя pKwpH pOH снижается от 14 10 до 11 22, а константа диссоциации аммиака при этом уменьшается с 1 8 - Ю-5 до 1 12 - КН. На рис. 3 изображен график изменения значения рН воды при различных температурах в зависимости от концентрации аммиака. [27]
Отсюда реакция вообще не должна идти при отсутствии ионов Н или ОН; если в нейтральной среде она все же, хотя и чрезвычайно медленно, протекает, то лишь постольку, поскольку и в нейтральном растворе присутствуют необходимые для ее протекания ионы водорода и гидроксила, образующиеся вследствие электролитической диссоциации воды. [28]
Вода служит не только средой ( например, растворяющей) для многих физических явлений, но и важнейшим агентом химических процессов выемной коре. Электролитическая диссоциация воды на катионы Н1 и анионы ( ОН) - и гидролиз связаны с образованием гидрооксидов, основных и кислых солей. Она способствует формированию гидрогелей в природе, протеканию метаморфических процессов и, в частности, перекристаллизации минеральных веществ. [29]
Но процесс коррозии возникает и в присутствии слабых электролитов и даже в присутствии воды. Степень электролитической диссоциации воды очень мала. [30]
Страницы: 1 2 3