Инверсия - конфигурация
Cтраница 1
Инверсия конфигурации столь типична для Зм2 - реакций, что стереохимическое понятие вальденовское обращение можно использовать как синоним данного механизма. [1]
 |
Стереохимия реакций нуклеофильного замещения крсмнийсодер. [2] |
Инверсия конфигурации наблюдается при замещении X в R3SiX, если X - Cl -, Br -, RCOO или ион n - толуолсульфоната. Считают, что замещение включает транс-ата. [3]
Инверсия конфигурации в первом случае и сохранение во втором случае соответствуют предсказаниям теории для четырех - и шестиэлектронных перициклических реакций, а также демонстрирует проявление стерических препятствий при образовании антараповерхностных переходных состояний. [4]
Инверсия конфигурации наблюдается не только для SN2 - pc - акций в растворе. Экспериментально было установлено, что и в газовой фазе бимолекулярное нуклеофильное замещение происходит с обращением конфигурации, например в реакции хлорид-иона с изомерными цис - и w / wwc - 4-бромциклогексанолами. [5]
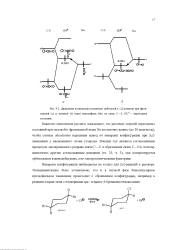 |
Диаграмма возмущения граничных орбиталей в й - реакции при фронтальной ( а и тыловой ( б атаке нуклеофила ( Nu на связь С-Z. ПС - переходное состояние. [6] |
Инверсия конфигурации наблюдается не только для бдй-реакций в растворе. [7]
Первоначально инверсию конфигурации в 5 2-реакциях объ-сняли чисто электростатическими факторами. В самом деле, в вреходном состоянии типа I несущие отрицательный заряд вхо-ящая и уходящая гругаш находятся на большем расстоянии друг друга, чем в переходном состоянии типа II, электростатичес-отгалкивание между этими группами в структуре I меньше, м в структуре II. Однако обращение конфигурации в реакции, шведенной на схеме 9.1, где входящая и уходящие группы за-сены разноименно и между ними должно быть электростати-жое притяжение, свидетельствует против простого объясне - t, основанного на электростатическом взаимодействии. В настоящее время инверсию в реакциях 3 объясняют в iMKax теории молекулярных орбиталей. В случае треугольного ходного состояния ( рис. 9.2, а) элементом симметрии, при-как связи C-Z, так и нуклеофилу и переходному состоя-является вертикальная зеркальная плоскость, проходящая переходном состоянии ПС) через центр нуклеофила и сере-связи C-Z. Относительно этой плоскости орбитали и и о ( етричны, а орбиталь ст антисимметрична. [8]
Первоначально инверсию конфигурации в - реакциях объясняли чисто электростатическими факторами. [9]
Карбанионы способны к инверсии конфигурации. [10]
При этом происходит инверсия конфигурации, но не наблюдается перераспределения дейтерия. В этом случае реакция сопровождается элиминированием, приводящим к образованию значительных количеств олефина. [11]
Наряду с этим инверсия конфигурации атома азота обусловливает существование равновесия между, например, двумя конфигурациями, подобными XXXV ( ф20) и XXXVI ( Ф 80), даже если взаимные переходы их путем вращения невозможны. [12]
В результате происходит полная инверсия конфигурации алкена эпоксида ( ji / t - цнклооктена образуется тране-циклооктен. [13]
Рассмотренный метод рекомендуется для инверсии конфигурации ациклических ди - и тризамещенных алкенов. Сильно экранированные эпоксиды очень медленно реагируют с ЛДФ, и поэтому алкены из них не удается получить с хорошими выходами. Наличие кетогруппы мешает реакции, поскольку тогда реагент расходуется ( 2 э / ce) на образование енолята. Эпокси-эфиры не удается дезоксигенировать с практически приемлемыми выходами. [14]
В работе [2] предполагается, что инверсия конфигурации происходит в процессе приобретения молекулой электрона. Так как протонизация обычно происходит с сохранением конфигурации, то промежуточный карбанион получается уже в инвертированной конфигурации. [15]
Страницы: 1 2 3 4