Вольфрамата
Cтраница 1
Вольфраматы растворяют в соляной кислоте, при этом выделяется нерастворимая вольфрамовая кислота. Шеелит CaW04 и вольфрамит ( Fe, Mn) W04 разлагают в азотной кислоте при нагревании. Шеелит растворяется в соляной кислоте довольно хорошо, он также хорошо растворяется в 10 % - ном растворе щавелевой кислоты и сплавляется с карбонатом натрия. [1]
Вольфраматы, состоящие из изоморфной смеси ферберита FeW04 и гюнберита MnW04, растврояют в соляной кислоте, иногда с добавкой хлората калия. Вольфрамовую кислоту из вольфрамовых руд и минералов выделяют хлорной кислотой. В смеси концентрированных серной и фосфорной кислот ( 4: 1) дымлением до паров разлагают силикатные минералы вольфрама. Бедные вольфрамовые руды сплавляют с карбонатом натрия с добавлением нитрата калия или пероксида натрия. [2]
Вольфраматы вполне устойчивы при обычных температурах. В природе вольфрам встречается главным образом в виде различных вольфраматов. [3]
Вольфраматы М2 Ю4 плавятся в интервале 600 - 1000 С без разложения. [4]
Вольфраматы являются производными вольфрамовой кислоты H2WO4, которая осаждается при действии минеральных кислот из растворов своих солей в виде белого осадка. Реакцию образования НДУО4 - Н О применяют для отделения WVI от других ионов. [5]
Вольфраматы являются производными вольфрамовой кислоты H2 VO4, которая осаждается при действии минеральных кислот из растворов своих солей в виде белого осадка. Реакцию образования H2WO4 - H2O применяют для отделения WVI от других ионов. С органическими кислотами H2WO4 образует комплексные соединения. [6]
Вольфраматы Ln2 ( WO4) 3 - nH2O получают при взаимодействии вольфраматов натрия с нитратами иттрия и лантаноидов в растворе. Вольфраматы РЗЭ нерастворимы в воде, спирте и ацетоне. Разбавленные минеральные кислоты, водные растворы щелочей при комнатной температуре действуют медленно. При 80 - 120 кислоты и щелочи растворяют их нацело, они не разлагаются до температур плавления. Все они изоструктурны и имеют моноклинную решетку. Физико-химические свойства средних вольфраматов описаны в [83, 84] и многих других работах. [7]
Вольфраматы получаются при реакциях в растворах, расплавах или твердых фазах. В зависимости от концентрации компонентов, среды и температуры процесса в результате синтеза или обменных реакций образуются нормальные, кислые ( изополивольфраматы) или основные соли. [8]
Вольфраматы получаются в растворах, расплавах или реакциями в твердых фазах. В зависимости от концентрации компонентов, среды и температуры процесса в результате синтеза или обменных реакций образуются нормальные, кислые ( изополивольфраматы) или основные соли. [9]
Вольфраматы, метаванадаты, соли сурьмы и ртути дают аналогичную реакцию. Влияние сурьмы и ртути устраняют восстановлением их медью. [10]
Вольфраматы являются производными вольфрамовой кислоты H2WO4, которая осаждается при действии минеральных кислот из растворов своих солей в виде белого осадка. Реакцию образования H2WO4 - H2O применяют для отделения WVl от других ионов. С органическими кислотами H2WO4 образует комплексные соединения. [11]
Вольфраматы являются производными вольфрамовой кислоты H2WO4, которая осаждается при действии минеральных кислот из растворов своих солей в виде белого осадка. Реакцию образования H2WO4 - H2O применяют для отделения Wvl от других ионов. С органическими кислотами H2WO4 образует комплексные соединения. [12]
Вольфраматы: нормальный WO, паравольфраматы tW6020 ( OH) ] 5 - и [ W12036 ( OH) 10P -, метавольфрамат [ W12038 ( OH) 2 ] - и г з-метавольфрамат [ W24012 ( OH) 12 ] 12 можно разделить электрофорезом на бумаге при напряжении 200 в за I час. [13]
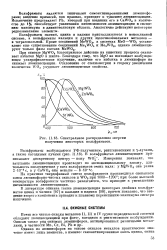 |
Спектральное распределение энергии излучения некоторых вольфраматов. [14] |
Вольфраматы являются типичными самоактивированными люминофо-рами; введение примесей, как правило, приводит к тушению люминесценции. Исключение представляет РЬ, который при введении его в CaWO4 в количестве до 1 % способствует увеличению интенсивности люминесценции и смещению максимума в длинноволновую область. Аналогично действуют некоторые редкоземельные элементы. [15]
Страницы: 1 2 3 4