Вольфрамата
Cтраница 3
Вольфраматы Pb ( II), Cu ( II), Mn ( II), Fe встречаются в земной коре в составе минералов. Изо-поли - и основные вольфраматы этих металлов мало изучены. [31]
Водные вольфраматы гафния и циркония при 700 С перегоняются с водяным паром без разложения. [32]
Моноклинные вольфраматы представлены главным образом рядом вольфрамита, в состав которого 1входят: ферберит - вольфрамат двухвалентного железа; гюбнерит - вольфрамат двухвалентного марганца и вольфрамит - изоморфная смесь двух предыдущих вольфраматов. Практически различие между тремя указанными минералогическими разностями до некоторой степени произвольно, так как ферберит содержит обычно немного вольфрамата марганца, а гюбнерит - вольфрамата железа. Все три разности сходны между собой по внешнему виду и металлическому блеску, ясно заметному на свежих поверхностях спайности; хрупкие и образуют неровный излом. Черта красная или шоколадно-коричневая ( отличие от касситерита, с которым они обычно встречаются); цвет от коричневого до черного. Притягиваются сильным электромагнитом ( ср. Тонко измельченный вольфрамит растворим в горячей соляной кислоте, азотной кислотой почти не разлагается. [33]
Вольфраматы РЗЭ того же состава представлены тремя изоструктур-ными сериями. [34]
Вольфраматы редкоземельных элементов ( р.з.э.) представляют собой труднорастворимые соединения. Выбор способа растворения или разложения их является важным этапом, от которого зависит дальнейший ход анализа. [35]
Вольфраматы щелочноземельных металлов, прежде всего кальция и бария, представляют значительный интерес для техники. Первый находит применение в технологии вольфрама, его соединений и сплавов и используется, как и второй, в радиоэлектронике. Вольфраматы кальция и стронция применяются в качестве люминофоров. Вольфраматы щелочноземельных элементов, за исключением MgWO 4, не растворимы в воде. Вольфрамат магния кристаллизуется в безводном состоянии в виде игл моноклинной системы. Образует два кристаллогидрата - с тремя и семью молекулами воды. [36]
Вольфраматы щелочноземельных металлов, прежде всего кальция и бария, представляют значительный интерес для техники. Первый находит применение в технологии вольфрама, его соединений и сплавов из руд и используется, как и второй, в радиоэлектронике. Вольфраматы кальция и стронция применяются в качестве люминофоров. Вольфраматы щелочноземельных элементов, за исключением MgWO4, не растворимы в воде. Вольфрамат магния кристаллизуется в безводном состоянии в виде игл моноклинной системы, образует два кристаллогидрата - с тремя и семью молекулами воды. [37]
Вольфраматы ряда металлов широко представлены в полиметаллических рудах, подвергаемых гидрометаллургической переработке. В аналитической химии труднорастворимые вольфраматы служат в качестве весовых форм при определении ряда металлов. [38]
Наиболее распространенные вольфраматы, описанные ниже, представляют соли вольфрамовой кислоты. Они отличаются средней твердостью, около 4 - 5, и высоким удельным весом. По генезису вольфраматы принадлежат к типичным минералам пневматолито-вых или гипотермальных жил; кроме того, они образуются при контактовых процессах. [39]
Вольфрамат, молибдат и оанадат ртути образуются на электроде в одних и тех же условиях. При любых соотношениях анионов в растворе катодные иолярограммы имеют один максимум тока, величина которого аддитивно складывается из токов электрохимического растворения соответствующих солей ртути. [40]
Вольфрамат кальция ( искусственный шеелит) обычно осаждают водным раствором хлористого кальция, добавляемого в раствор вольфрамата натрия. [41]
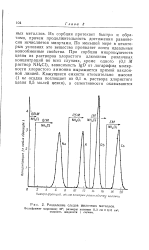 |
Разделение следов щелочных металлов. [42] |
Вольфрамат циркония; 25; размеры колонки 11 3 еж X 0 13 см2; скорость жидкости 1 см / мин. [43]
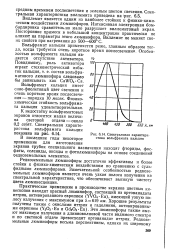 |
Спектральная характеристика вольфрамата кальция. [44] |
Вольфрамат кальция применяется реже, главным образом тогда, когда требуется очень короткое время послесвечения. Особенностью вольфрамата кальция является отсутствие активатора. [45]
Страницы: 1 2 3 4