Ингибирование - фермент
Cтраница 2
 |
Необратимое ингибирование фермента иодуксусной кислотой. Иод вступает в реакцию с сульфгидрильными группами фермента. [16] |
Некоторые вещества вызывают необратимое ингибирование ферментов. Рассмотрим два примера такого рода. [17]
Кинетическая характеристика реакций ингибирования ферментов базируется на представлениях о механизме взаимодействия ингибиторов с ферментами. [18]
Представления относительно кинетики ингибирования ферментов в присутствии субстрата были использованы при исследовании взаимодействия холинэстераз с фосфорорганическими ингибиторами. Результаты сопоставления теории с опытными данными, а также дальнейшее развитие теории будут даны в гл. [19]
Некоторые воздействия не вызывают ингибирования ферментов, а повышают их активность. Поскольку эти энзимы выражены преимущественно в тканях, где трудно взять образцы для биопсии, активность ферментов определяется косвенно in vivo путем введения вещества, метаболизируемого конкретным ферментом, а затем продукт распада измеряется в моче или плазме. [20]
Конкурентное ингибирование - тип ингибирования фермента, которое можно снять, повысив концентрацию субстрата. [21]
Неконкурентное ингибирование - тип ингибирования ферментов, которое не снимается при повышении концентрации субстрата. [22]
Известны и другие типы ингибирования ферментов, рассмотрение которых выходит за рамки этого курса. [23]
 |
Тонкослойно-хроматографическое определение пестицидов ингибированием ферментов. [24] |
Показано [121, 123], что метод тонкослойно-хромато-графического ингибирования ферментов по чувствительности значительно превосходит метод химического определения пестицидов и не уступает трудоемкому биологическому методу. [25]
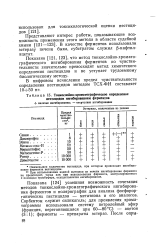 |
Тонкослойно-хроматографическое определение пестицидов ингибированием ферментов. [26] |
При использовании водной вытяжки из печени ингибирование фермента не происходит, тогда как при использовании фермента, экстрагированного с помощью трисбуфера, осуществляется ингибирование. [27]
Уоткинс и Морган [4], изучая ингибирование фермента сахарами, получили дополнительные и независимые доказательства роли, которую играют L-фуко-за, N-ацетилгалактозамин и D-галактоза в Н -, А - и В-специфичности. Известно, что действие фермента может быть подавлено избытком одного из продуктов реакции. Из Trichomonas foetus удалось получить фермент, разрушивший субстраты, состоявшие из А -, В - и Н - веществ. [28]
Вопрос об интерпретации термодинамических констант реакций ингибирования ферментов столь же сложен, как и для реакций с субстратами, и в литературе освещен в еще меньшей степени. Имеющиеся экспериментальные данные о термодинамике взаимодействия холинэстераз с ингибиторами типа четвертичных солей алкиламмония говорят о важной роли энтропийного фактора в этом процессе, что свидетельствует о значении анионных центров фермента в поддержании его трехмерной структуры, необходимой для организации активного центра ( см. стр. [29]
Такими побочными реакциями, конкурирующими с ингибированием фермента, являются спонтанный гидролиз субстрата, гидролиз ингибитора, вызываемый содержащимися в ферменте фосфорилфосфа-тазами, адсорбция на стенках стеклянного сосуда при работе с очень разбавленными растворами, реакция с другими активными группами присутствующих белков. Кроме того, в случае слабого ингибитора одновременно протекают и угнетение, и реактивация фермента. [30]
Страницы: 1 2 3 4