Ингибирование - фермент
Cтраница 4
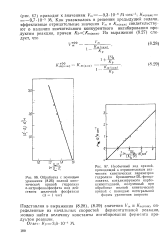
Подставляя в выражения (8.28), (8.29) значения Vm и / С Г1 ( каж), определенные из начальных скоростей ферментативной реакции, можно найти величину константы ингибирования фермента продуктом реакции. [47]
В этом разделе кратко рассмотрены общие факторы, в частности зависимость скорости ферментативной реакции от времени, влияние концентраций субстрата и фермента на скорость реакций, катализируемых ферментами, и более подробно - вопросы об активировании и ингибировании ферментов. Ранее была отмечена существенность для активности ферментов таких факторов, как температура, рН, т.е. факторов, которые определяют в оптимальных условиях сохранность пространственной конфор-мации молекулы фермента, когда она приобретает максимальную активность. [48]
В моче человека можно обнаружить активность ряда ферментов: липазы, рибонуклеазы, ЛДГ, аминотрансфераз, урокиназы, фосфатаз, а-амила-зы, лейцинаминопептидазы и др. Основные трудности при определении активности ферментов мочи, кроме а-амилазы и некоторых других, заключаются в необходимости сгущения ( концентрирования) мочи и предотвращении ингибирования ферментов в процессе этого сгущения. [49]
Реакция in vitro всех остальных соединений, более ценных как инсектициды, гораздо слабее и, кроме того, они значительно медленнее гидролизуются щелочью. Скорости ингибирования фермента in vitro и щелочного разложения коррелируют положительно. Димефокс и шра / дан, особенно последний, настолько малоактивны для холинэстеразы in vitro, что их трудно считать токсичными, но после обработки окислителями в течение достаточно продолжительного времени они становятся сильными ингибиторами. Избыточное окисление или длительное хранение в водном растворе после слабого окисления вновь разрушает их активность. Установлено, что и в тканях насекомых, и в печени животных образуются те же самые промежуточные активные вещества. [50]
Разбираются причины гибели животных и приводятся данные по снижению уровня холинэстераз в разных органах и тканях в различное время после действия зарина, ДФФ и других фосфорорганических ингибиторов, а также постепенное спонтанное восстановление активности ферментов под действием реактиваторов. Разбирается механизм ингибирования ферментов, обладающих эстеразной активностью, и накопление в тканях насекомых ацетилхолина при действии фосфорорганических веществ. [51]
Группа французских исследователей впоследствии представила ( результаты физико-химического изучения гексокиназы, которые в некоторой степени подтверждают их гипотезу об упорядоченном механизме. Подробное исследование ингибирования фермента позволило Косоу и Роузу [94] заключить, что при некоторых условиях ( малые или умеренные ингибирующие концентрации МдАДФ -) продукты реакции выделяются в определенной последовательности - сначала глкжозо-6 - фоофат, а затем АДФ. [52]
Ингибирование фтором может носить конкурентный, неконкурентный и смешанный характер [ Cimasoni G. Часто происходит также ингибирование ферментов, активируемых металлами, особенно Mg2, причем оно может усиливаться фосфатами, как, например, в случае энолазы и сункцинатдегид-рогеназы. Известны, однако, и металлактивируемые ферменты, не ингибируемые фтором. Подобным же образом фтор способен ингиби-ровать и другие ферменты, особенно если в их активном центре содержатся положительно заряженные остатки лизииа и аргинина. [53]
Страницы: 1 2 3 4