Стерическое ингибирование
Cтраница 1
Стерическое ингибирование тс-р-сопряжения хорошо иллюстрируется на примере замещенных М - диалкиланилинов ( Remington, 1945; Klevens, Platt, 1949), Введение о-заместителей приводит к исчезновению полосы вблизи 2500 А, приписываемой хромофору С & Н5 - N:, причем степень уменьшения интенсивности согласуется с размерами заместителя. [1]
Наиболее ярким примером стерического ингибирования реакционной способности в реакциях SN1 является, пожалуй, инертность триптицилбромида ( ЬХУ) ( Bartlett, Lewis, 1950; ср. [2]
Определенную роль, возможно, играет и стерическое ингибирование эндо-атакн, например, в системе бицикло [2,2,1] гептана69, а также природа растворителя. [3]
Эта разница ( 12 3 CMS) должна быть приписана очень сильному стерическому ингибированию мезомерии в первом соединении ( ср. Если сравнить эту разницу с экзальтацией в нитробензоле и в Г Г М - ди-метиланилине-соответствен но около 0 9см3 и 1 7 см3 ( ср. [4]
Основанием для такого разделения является, конечно, тот факт, что стерическое ингибирование мезомерии в 2-нитро-изомере ( LXXXVI) вызывает уменьшение скорости гидролиза по сравнению с 6-нитроизомером ( LXXXIV), в котором такое ингибирование отсутствует ( ср. [5]
Как будет показано ниже, несомненно, что в этой молекуле имеется значительное стерическое ингибирование мезомерии. [6]
В настоящей главе кратко рассмотрены также различные кинетические стерические эффекты-пространственной затрудненности, стерического ускорения и, наконец, стерического ингибирования сопряжения в гемолитических реакциях. [7]
Так, 4-нитро - З - хлорацетанилид деацилируется в три раза быстрее, чем 4-нитроацетанилид, а о наличии небольшого стерического ингибирования мезомерии можно только заключить на основании того факта, что 2-нитро - 5-хлорацетанилид реагирует приблизительно в десять раз быстрее, чем 2-нитроацетанилид. [8]
Геометрические изомеры соединений, включающих сопряженную систему кратных связей, заметно различаются по спектральным параметрам / ( - полосы из-за проявления стерического ингибирования сопряжения в чыс-изомере. С ИзЬмере имеют более высокие значения, чем в ч с-изомере ( см. табл. 2.3, ср. [9]
Цианофенолы были включены в это исследование, чтобы ш-т казать, что в случае нитрофенолов большая часть АрД й действительно обусловлена стерическим ингибированием мезомерии. Поскольку циан-группа линейна, она не может быть серьезны препятствием для мезомерного взаимодействия. Небольшая, в - личина наблюдаемых разностей является серьезным доказатель / -, ством правильности предложенной интерпретации. [10]
Здесь, однако, в отличие от фенолов мезомерное взаимодействие будет сильнее в кислоте, чем в анионе, и, таким образом, стерическое ингибирование мезомерии поведет к увеличению кислотности. [11]
Как уже отмечалось, эти напряжения в ионе должны уменьшаться; поэтому следует ожидать, что основность будет больше, чем у М М - диметиланилина, несмотря на отсутствие стерического ингибирования мезомерии. [12]
Данные, полученные при исследовании ультрафиолетовых спектров, молекулярной рефракции и относительных скоростей гидролиза и-этоксикарбонильных производных, позволили прийти к следующим выводам: а) во всех простых производных анилина и N-метиланилина с одной алкильной группой в орто-положении не наблюдается стериче-ского ингибирования резонанса, независимо от характера алкильной группы; б) у производных N-метиланилина с двумя о-алкиль-ными группами и производных К - диметиланилина, по крайней мере, с одной алкильной группой в орто-положении имеет место стерическое ингибирование резонанса, степень которого зависит от эффективного объема алкильной группы. Такой анализ был использован затем для определения факторов, от которых зависит основность этих соединений; данные, приведенные в табл. 6.8, выбраны из обширного материала Уэпстера. [13]
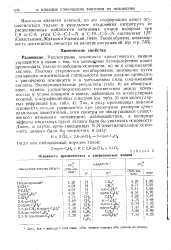 |
Основность ароматических и алифатических аминов. [14] |
Рассмотрение основности ароматических аминов упрощается в связи с тем, что мезом рное взаимодействие может происходить только в свободном основании, но не в сопряженной кислоте. Поэтому стерическое ингибирование мезомерии путем понижения относительной стабильности амина должно приводить к увеличению основности и к уменьшению силы сопряженной кислоты. Так, в ряду производных анилина основность сильно уменьшается при увеличении размеров орпго-алкильных заместителей, хотя спектры не обнаруживают существенного изменения мезомерного взаимодействия, - а полярные эффекты алкильных групп должны были бы увеличить основность. [15]
Страницы: 1 2 3