Индикатор - гаммет
Cтраница 2
Наиболее доступным методом определения общей кислотности гетерогенных катализаторов является метод аминного титрования. Он состоит в адсорбции органического основания из неполярных растворителей в присутствии индикаторов Гаммета. Так как адсорбированные на кислотных центрах молекулы индикатора при этом замещаются титрующим амином, молекулы последнего должны быть более сильным основанием, чем индикатор. [16]
Бранд и сотрудники [36] использовали ароматические нитросоедине-ния как индикаторные основания для того, чтобы распространить шкалу Я0 далеко в область олеума, и получили значения основности, которые из-за сольволитических эффектов немного отличаются от значений, полученных ими ранее. Моно - и динитробензолы, а также моно - и динитротолуо-лы являются ценными индикаторами Гаммета в интервале кислотностей всего олеума. Тринитробензол не проявляет основных свойств по отношению к H2S2O7 [40, 73] - среде достаточной кислотности для того, чтобы протонировать даже серу и иод. Это означает, что 1 3 5-тринитробензол мы можем в будущем использовать для изучения сред с еще большей кислотностью, когда такие среды станут доступными. [17]
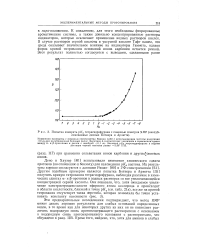 |
Попытка измерить рКа тетрагидрофурана с помощью спектров ЯМР ( неопубликованные данные Ботнера и Ариетта. [18] |
К сожалению, для этого необходимы фторированные ароматические системы, а также довольно концентрированные растворы индикаторов, которые исключают применение водных растворов кислот. В случае растворов серной кислоты в уксусной кислоте Тафт нашел, что среда оказывает значительное влияние на индикаторы Гаммета, однако форма кривой титрования оснований ионов карбония остается резкой. [19]
Таким образом, предстоит еще многое сделать для того, чтобы существующие сейчас общие представления о природе активных центров стали более конкретными. До сих пор противоречивые результаты получены при количественном измерении числа и силы кислотных центров с различной структурой, в частности путем титрования с индикаторами Гаммета. Эти исследования необходимо продолжить, поскольку полученные данные не могут объяснить причины более высокой активности цеолитов, в особенности активности в реакциях превращения парафиновых углеводородов, по сравнению с другими кислотными гетерогенными катализаторами, такими, как аморфные алюмосиликаты. Возможно, что в будущем станет более понятно, связана ли повышенная каталитическая активность цеолитов с более высокой концентрацией кислотных центров, с большей силой кислотности отдельных центров или с особенностями кристаллической структуры. Во всяком случае до сих пор, но-видимому, не получено данных о том, что цеолиты обладают более сильными кислотными центрами, чем другие катализаторы. [20]
Взаимодействие нитрогруппы с карбоксильными группами, как наблюдалось, сводит к нулю все изменения в спектре после протонирования. Так, например, найдено, что ни / г-нитробензойная кислота [113], ни / г-нитро-бензамид [100] нельзя изучать как слабые основания по методу индикаторов Гаммета. [21]
Цеолит NH4X изучен значительно меньше, отчасти это обусловлено тем, что он значительно менее стабилен, особенно при высоких степенях обмена. Титрование с индикаторами Гаммета показало, что после термообработки цеолит NH4X значительно уступает цеолиту Y как по числу, так и по силе кислотных центров [98, 103], хотя из-за более высокого содержания алюминия в цеолите Y больше ионов NtTj. Каталитическая активность НХ обычно ниже, чем у HY. [22]
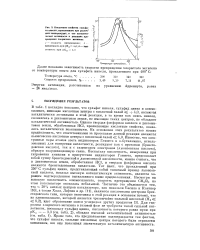 |
Кислотные свойства сульфата никеля, прокаленного при различных температурах, и его каталитическая активность в реакциях превращения хлористого метилена. [23] |
В табл. 1 наглядно показано, что сульфат никеля, сульфид цинка и алюмосиликат, имеющие кислотные центры с кислотной силой 4 0, являются каталитически активными в этой реакции, в то время как окись никеля, силикагель и диатомитовая земля, не имеющие таких центров, не обладают каталитической активностью. Однако твердая фосфорная кислота и диатомитовая земля, обработанная НС1, проявляющие кислотные свойства, оказались каталитически неактивными. Известно, что электронные пары атомов азота индикаторов Гаммета и м-бутиламина, использованных для измерения кислотности, реагируют как с протоном ( бренсте-довская кислота), так и с акцептором электронов ( лыоисовская кислота), образуя координационную связь. Поскольку кислотность, измеренная при титровании аминами в присутствии индикаторов Гаммета, представляет собой сумму, бренстедовской и льюисовской кислотности, можно считать, что и диатомитовая земля, обработанная НС1, и твердая фосфорная кислота являются бренстедовскими кислотами. Тот факт, что прокаленный при 350 С сульфид цинка, представляющий собой типичный пример льюисовской кислоты, показал высокую каталитическую активность, является хорошим подтверждением высказанного выше предположения. Несмотря на высокую кислотность алюмосиликата, скорость превращения СН2С12 на этом катализаторе оказалась небольшой. Кроме того, это предположение подтверждается тем фактом, что сульфат никеля, сильные кислотные центры которого были отравлены хинолином, все еще показывал значительную каталитическую активность. [24]
В трех последних столбцах табл. 8 приведены рассчитанные для растворов, содержащих 1 М воды, отношения безводных или гидратированных ионов к аналитически определенной концентрации ионов. Если в ацетонитриле содержится 1 М воды, то лишь 17 % ионов натрия присутствуют в дегидратированной форме, 33 % - в виде моногидрата и 50 % - в виде дигидрата. Особенно интересно отметить, что протонированная форма индикатора Гаммета, ж-нитроанилин, имеет большую константу гидратации. При концентрации воды 1М только 14 % индикатора находится в дегидратированной форме, 72 % - в виде моногидрата и 14 % - в виде дигидрата. Протонированные формы других индикаторов Гаммета, несомненно, гидратированы столь же сильно. Существенно то, что катионы индикатора Гаммета сильнее сольватируются в воде, чем в ацетонитриле. По этой же причине функция кислотности Гаммета не может быть использована для точного определения значения коэффициента распределения протона между водой и ацетонитрилом. [25]
Алифатические амиды имеют сильную полосу поглощения карбонильной группы в области 2000 ммк, которая сильно изменяется с повышением кислотности среды. Гольдфарб с сотрудниками [143, 144] предприняли попытку с помощью этого явления измерить основности многих алифатических амидов, пептидов и протеинов в водном растворе серной кислоты. Если предположить, что эти соединения являются хорошими индикаторами Гаммета, то эти данные, по-видимому, означают, что многие из изученных соединений имеют два значения р / С0; это попытались объяснить с помощью равновесия образования водородной связи. Таким образом, данные Гольдфарба можно будет рассматривать лишь после того, как это явление будет понято; Эдвард и Уанг [102] объясняют такое поведение амидов при помощи различий в гидратации амидов и индикаторов Гаммета. [26]
Низкая основность и довольно высокая диэлектрическая проницаемость ( - 40) делают нитрометан очень интересным растворителем для неводного титрования. Гаммету и его ученикам [317, 348] удалось построить довольно хорошую шкалу Н0, используя смеси нитрометана с серной кислотой, хотя из-за слабой способности к сольватации наблюдается значительная ассоциация. Найдено, что в отсутствие гидроксилсодер-жащего растворителя сам индикатор Гаммета, используемый для изучения системы, вынужден сольватировать образующиеся бисульфат-анионы. Поведение системы здесь совершенно иное, чем в спиртовых растворах, действие которых подобно действию воды, хотя их диэлектрические проницаемости могут быть ниже диэлектрической проницаемости нитрометана. [27]
Следовательно, такой подход является довольно грубым приближением, возможно, за исключением растворителей с высокими диэлектрическими постоянными. Ниже дается пример большого различия коэффициента распределения протона между водой и диметилсульфоксидом, выведенного из функции кислотности Гаммета и постоянства потенциала системы ферроцен-ферри-цин. В табл. 8 приведен другой пример сильной гидратации кислотной формы индикатора Гаммета при введении небольших количеств воды в ацетонитрил ( АН), показывающий, что сольватация индикаторного катиона происходит значительно сильнее в воде, чем в ацетонитриле. [28]
В табл. 1 наглядно показано, что сульфат никеля, сульфид цинка и алюмосиликат, имеющие кислотные центры с кислотной силой 4 0, являются каталитически активными в этой реакции, в то время как окись никеля, силикагель и диатомитовая земля, не имеющие таких центров, не обладают каталитической активностью. Однако твердая фосфорная кислота и диатомитовая земля, обработанная НС1, проявляющие кислотные свойства, оказались каталитически неактивными. Известно, что электронные пары атомов азота индикаторов Гаммета и м-бутиламина, использованных для измерения кислотности, реагируют как с протоном ( бренсте-довская кислота), так и с акцептором электронов ( лыоисовская кислота), образуя координационную связь. Поскольку кислотность, измеренная при титровании аминами в присутствии индикаторов Гаммета, представляет собой сумму, бренстедовской и льюисовской кислотности, можно считать, что и диатомитовая земля, обработанная НС1, и твердая фосфорная кислота являются бренстедовскими кислотами. Тот факт, что прокаленный при 350 С сульфид цинка, представляющий собой типичный пример льюисовской кислоты, показал высокую каталитическую активность, является хорошим подтверждением высказанного выше предположения. Несмотря на высокую кислотность алюмосиликата, скорость превращения СН2С12 на этом катализаторе оказалась небольшой. Кроме того, это предположение подтверждается тем фактом, что сульфат никеля, сильные кислотные центры которого были отравлены хинолином, все еще показывал значительную каталитическую активность. [29]
Алифатические амиды имеют сильную полосу поглощения карбонильной группы в области 2000 ммк, которая сильно изменяется с повышением кислотности среды. Гольдфарб с сотрудниками [143, 144] предприняли попытку с помощью этого явления измерить основности многих алифатических амидов, пептидов и протеинов в водном растворе серной кислоты. Если предположить, что эти соединения являются хорошими индикаторами Гаммета, то эти данные, по-видимому, означают, что многие из изученных соединений имеют два значения р / С0; это попытались объяснить с помощью равновесия образования водородной связи. Таким образом, данные Гольдфарба можно будет рассматривать лишь после того, как это явление будет понято; Эдвард и Уанг [102] объясняют такое поведение амидов при помощи различий в гидратации амидов и индикаторов Гаммета. [30]
Страницы: 1 2 3