Восстановление - перекись
Cтраница 1
Восстановление перекисей, полученных из фенантрена, иоди-стоводородной кислотой дает 2, 2 -диальдегид дифенила. [1]
Восстановление перекисей и гидроперекисей с помощью 1ЛА1Н4 может быть использовано с аналитическими целями. [2]
Восстановление перекисей, полученных из фенантрена, иоди стоводородной кислотой дает 2, 2 -диальдегид дифенила. [3]
Восстановление перекисей диоксимов ( фуроксанов, окисей изоксадиазолов до оксимов ( N2O8) - 2NOH ( стр. [4]
При восстановлении перекисей могут образоваться следы альдеги-дя. Если требуется эфир высшей степени очистки, то встряхивают его с 0 5 % - ньш раствором перманганата калия ( окисление альдегида в кислоту), затем с 5 % - ним раствором едкого натра и, наконец, с водой, после чего следуют высушивание и перегонка. [5]
При восстановлении перекисей могут образоваться следы альдегида. Если требуется эфир высшей степени очистки, то встряхивают его с 0 5 % - ным раствором перманганата калия ( окисление альдегида в кислоту), затем с 5 % - ным раствором едкого натра и, наконец, с водой, после чего следует высушивание и перегонка. [6]
При восстановлении перекисей могут образоваться следы альдегида. Если требуется эфир высшей степени очистки, то встряхивают его с 0 5 % - ным растворам перманганата калия ( окисление альдегида в кислоту), затем с 5 % - ным раствором едкого натра и, наконец, с водой, после чего следуют высушивание и перегонка. [7]
При восстановлении перекисей могут образоваться следы альдегида. Если требуется эфир высшей степени очистки, то встряхивают его с 0 5 % - ным раствором перманганата калия ( окисление альдегида в кислоту), затем с 5 % - ным раствором едкого натра и, наконец, с водой, после чего следуют высушивание и перегонка. [8]
Метод основан на восстановлении перекиси бензоила на ртутном капельном электроде-катоде в водно-ацетоновой среде на фоне хлористого лития и азотнокислого калия. [9]
Таким образом, потенциал восстановления настоящих перекисей практически отождествляется с потенциалом обратимого восстановления иона водорода. Бернард, изучив большое число различных перекисей, показал возможность полярографического определения одновременно нескольких перекисей в смеси. [10]
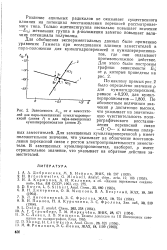 |
Зависимость. / от ст заместите. [11] |
Различие ацильных радикалов не оказывает существенного влияния на потенциал восстановления перекисей рассматриваемого типа. [12]
В случае капельного электрода каталитическая волна почти сливается с волной восстановления перекиси, поэтому она труднодоступна для измерения. Далее, для сохранения псевдомономолекулярного характера реакции необходимо применять очень низкие концентрации ионов железа, но при этом начинает сказываться каталитическое действие железа, присутствующего в щелочах в виде примесей. При полярографи-ровании со струйчатым электродом можно работать с большими концентрациями Fe3, и, поскольку потенциал полуволны перекиси водорода на этом электроде сдвинут приблизительно на 0 3 в в сторону отрицательных потенциалов, величина каталитического тока легче поддается измерению. [13]
В случае капельного электрода каталитическая волна почти сливается с волной восстановления перекиси, поэтому она труднодоступна для измерения. Далее, для сохранения псевдомономолекулярного-характера реакции необходимо применять очень низкие концентрации ионов железа, но при этом начинает сказываться каталитическое действие железа, присутствующего в щелочах в виде примесей. При полярографи-ровании со струйчатым электродом можно работать с большими концентрациями Fe3, и, поскольку потенциал полуволны перекиси водорода на этом: электроде сдвинут приблизительно на 0 3 в в сторону отрицательных потенциалов, величина каталитического тока легче поддается измерению. [14]
В этом случае происходит каталитическое разложение, а не процесс восстановления перекиси. Перекись эфира ведет себя при этом так же, как и алкиль-ные перекиси, которые под влиянием солей претерпевают каталитическое расщепление. [15]
Страницы: 1 2 3