Восстановление - тетрахлорид
Cтраница 1
Восстановление тетрахлорида гермическим путем производят в защитной атмосфере аргона. Восстановителями служат магний или натрии. Наиболее распространен магнийтермический метод Кроля. [1]
Восстановление тетрахлоридов магнием лежит в основе хорошо известного процесса Кролля для получения таких химически активных металлов, как титан и цирконий. [2]
Восстановление тетрахлорида циркония магнием проводится в среде аргона или гелия в той же установке, что и очистка. Сначала расплавляют магний, а затем возгоняют терахлорид циркония, который вступает в реакцию с магнием. Реакция восстановления тетрахлорида циркония магнием экзотермична, поэтому скорость ее нужно строго контролировать, меняя скорость испарения тетрахлорида соответствующим регулированием температуры. [3]
Для восстановления тетрахлоридов этих металлов применяют амальгамы щелочных, щелочноземельных металлов или их смеси. Восстановление проводят под давлением в реакторе, куда подают нагретый до 300 С тетрахлорид титана и нагретую до 400 С натриевую амальгаму, содержащую около 3 % натрия; температуру в реакторе поддерживают 500 - 700 С. При этом образуется галогенид натрия и тонкодисперсный металлический титан, который в свою очередь образует со ртутью интерметаллическое соединение TiHg и отделение которого от ртути не представляет затруднений. В качестве восстановителей применяют также трех-компонентные амальгамы, которые, кроме натрия или калия, содержат металл, образующий низкоплавкую эвтектику с восстанавливаемым тугоплавким металлом или с хлоридом металла восстановителя. [4]
Для восстановления тетрахлоридов этих металлов применяют амальгамы щелочных, щелочноземельных металлов или их смеси. Восстановление проводят под давлением в реакторе, куда подают нагретый до 300 С тетрахлорид титана и нагретую до 400 С натриевую амальгаму, содержащую около 3 % натрия; температуру в реакторе поддерживают 500 - 700 С. При этом образуется галогенид натрия и тонкодисперсный металлический титан, который в свою очередь образует со ртутью интерметаллическое соединение TiHg и отделение которого от ртути не представляет затруднений. В качестве восстановителей применяют также трех-компонентные амальгамы, которые, кроме натрия или калия, содержат металл, образующий низкоплавкую эвтектику с восстанавливаемым тугоплавким металлом или с хлоридом металл а восстановителя. [5]
Экспериментально изучено восстановление тетрахлоридов кремния, германия и титана, хлорида и фторида бора, хлоридов тантала и ниобия. В настоящее время накоплен известный опыт получения порошков тугоплавких карбидов, нитридов, бо-ридов, силицидов в низкотемпературной плазме. [6]
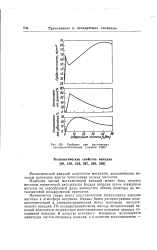 |
Свойства при растяжении ванадиевотитановых сплавов. [7] |
Применяется также метод восстановления тетрахлорида ванадия магнием в атмосфере водорода. Однако более распространены каль-циетермический и алюминотермический метод получения металлического ванадия. По кальциетермическому методу металлический ванадий получается посредством восстановления кальцием окисных соединений ванадия. [8]
Недавно был разработан метод восстановления тетрахлоридов циркония и гафния в промышленном масштабе с применением вместо магния металлического натрия. Основным преимуществом метода восстановления натрием является, по-видимому, его более низкая стоимость. В том случае, когда для восстановления тетрахлорида гафния применяется натрий, за операцией восстановления следует выщелачивание продукта реакции водой с целью удаления солей и избытка натрия из губчатого гафния. [9]
Наиболее чистый кремний получают восстановлением тетрахлорида кремния водородом или цинком. [10]
Мельников [11], изучая процесс восстановления тетрахлоридов кремния и германия с целью получения поликристаллических пленок, обратил внимание на важную роль в этом процессе водорода. Оказалось, что количество водорода, необходимого для получения качественных осадков, должно на два порядка превышать его концентрацию, соответствующую стехиометрии реакции восстановления. [11]
Кремниевые покрытия наносятся на металлы восстановлением тетрахлорида кремния водородом; например, таким способом можно силицировать сталь и молибден. [12]
Сернистый водород сначала обесцвечивает раствор вследствие восстановления тетрахлорида в трихлорид иридия, сопровождающегося выделением серы; после этого осаждается бурый IraSs, легко растворимый в ( NH S. Из всех платиновых металлов иридий наиболее трудно осаждается сероводородом. Он легче осаждается из солянокислых, чем из хлорнокислых растворов. [13]
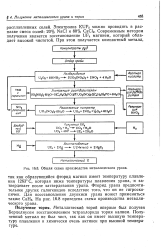 |
Общая схема производства металлического урана. [14] |
Металлический торий впервые был получен Берцелиусом восстановлением тетрахлорида тория калием. Полученный металл не был чист, гак как он имеет высокую температуру плавления и химически очень активен при высокой температуре. [15]
Страницы: 1 2 3 4