Восстановление - церие
Cтраница 2
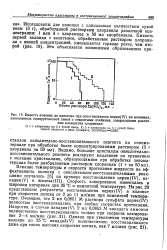
Например, при титровании ионов ванадила раствором сульфата церия ( IV) кривая титрования имеет вид, изображенный на рис. 7: вначале повышение силы тока обусловлено восстановлением ванадия ( V), образующегося во время титрования ( за счет окисления ванадила церием), а затем, после точки эквивалентности, - восстановлением избыточного церия. Так как коэффициенты диффузии ионов V03 и Се4 различны, то различен и наклон кривой титрования до и после конечной точки. [16]
Например, при титровании ионов ванадила раствором сульфата церия ( IV) кривая титрования имеет вид, изображенный на рис. 7: вначале повышение силы тока обусловлено восстановлением ванадия ( V), образующегося во время титрования ( за счет окисления ванадила церием), а затем, после точки эквивалентности, - восстановлением избыточного церия. Так как коэффициенты диффузии ионов VO3 и Се4 различны, то различен и наклон кривой титрования до и после конечной точки. [17]
Осмий и рутений в восьми - и четырехвалентном состоянии в сильной степени катализируют реакцию между мышьяком ( III) и солями церия ( IV) в кислых растворах: сама по себе эта реек-ция протекает крайне медленно 13, но она катализируется иодом, и в литературе описан фотометрический метод определения иода, основанный на измерении скорости восстановления церия ( IV) избытком арсенитаи. Каталитический эффект осмия даже более сильный, чем иода; он заметен уже при нескольких тысячных долях микрограмма осмия в 5 мл раствора. Хлориды уменьшают каталитическую способность осмия, и поэтому количество их в растворе надо контролировать. [18]
Двуокись церия растворяется в концентрированной азотной кислоте при нагревании до кипения. Для восстановления церия до трехвалентного в раствор периодически добавляется перекись водорода. [19]
 |
Концентрационные волны в реакции Белоусова ( а и вложенные волны в реакции Белоусова ( б. [20] |
Реакция окисления церия является автокаталической, т.е. продукты реакции являются ее катализаторами. Сначала протекает медленная реакция восстановления церия, так как Вг - действует как сильный замедлитель. Затем процесс повторяется сначала. Так как избыток Се3 1 окрашивает раствор в красный цвет, а избыток Се4 1 окрашивает раствор в синий, наблюдается периодическое изменение цвета раствора. Колебания будут происходить до тех пор, пока не будут израсходованы все реактивы реакции. При протекании этих химических реакций в тонком слое будет иметь место образование пространственно-временных структур, которые имеют форму кольцевых или спиральных волн. Спиральные волны образуются при разрыве плоских или кольцевых волн. Источники кольцевых волн называются ведущими центрами, которые возникают в результате случайных флуктуации концентраций. [21]
 |
Емкость колонки до проскока при восстаяовлении церий ( 1У на колонках, заполненных лолиуретаяовой пеной с открытыми ячейками, содержащими различные количества хлоранила. [22] |
На рис, 20 представлены результаты восстановления церия ( IV) в колонке при скоростях потока от 2 до 11 мл / мин при комнатной температуре. Очевидно, что 2 мл 0 0851 М раствора сульфата церия ( IV) полностью восстанавливались при любых скоростях протекания. [23]
Первоначально этот ток будет поддерживаться постоянным благодаря процессу восстановления церия ( IV), поскольку предельный ток на кривой А превышает пропускаемый ток. По мере продолжения электролиза предельный ток восстановления церия ( IV) падает ниже i, и эффективность тока становится меньше 100 %; потенциал катода резко сдвигается до значения, при котором происходит другая электродная реакция - восстановление иона водорода при потенциале - 0 В - сила тока поддерживалась постоянной. Если первоначально выбран ток большей силы - 12, катод немедленно приобретает потенциал, при котором одновременно выделится газообразный водород, тем самым эффективность тока восстановления церия ( IV) станет меньше 100 % с самого начала электролиза. К тому же даже, если церий ( IV) непосредственно не реагировал бы на платиновом катоде, он химически восстанавливается газообразным водородом, поэтому суммарный результат был бы тот же, что и при восстановлении церия ( IV) со 100 % - ной эффективностью тока. Однако, поскольку газообразный водород не реагирует с церием ( IV) с измеряемой скоростью, кулонометрическое титрование церия ( IV) при постоянной силе тока не удается провести в этих условиях. [24]
В качестве примера рассмотрим процесс восстановления Се1У в 1 М растворе KfoSO Под действием тока постоянной силы CeIV восстанавливается до Сеш. Однако в процессе электролиза предельная сила тока восстановления церия становится меньше налагаемой силы тока; в этих условиях сила тока поддерживается благодаря восстановлению ионов водорода. Газообразный водород не сразу начинает взаимодействовать с церием ( IV), поэтому некоторое количество электричества расходуется на вторичный процесс, и зависимость Q от количества церия не подчиняется закону Фарадея. [25]
Таким же образом осаждаются Zr и Се4, но иодаты трехвалентных редкоземельных элементов легко растворяются в HNOS. Для того чтобы избавиться от Се4, прибавляют Н202 для восстановления церия в трехвалентный. [26]
Монацитовый песок ( 5 г) разлагают серной кислотой, как рбычно, и отделяют торий вместе с редкоземельными элементами при помощи щавелевой кислоты. Прокаленный осадок растворяют в Соляной кислоте ( 1: 1), добавляют перекись водорода для восстановления церия ( IV) и празеодима ( IV), переносят раствор в мерную колбу емкостью 100 мл и доводят объем до метки водой. Берут аликвотные часта по 1 - 3 мл, создают рН раствора 2 - 3 ( при помощи аммиака), доводят объем до 10 - 20 мл водой и титруют 0 06 М раствором ЭДТА. [27]
Смит и Гетц [378] установили, что азотно - и хлорно-кислотные растворы церия ( 1У) нельзя хранить на свету, так как при этом концентрация церия ( 1У) уменьшается на 0 01 - 0 03 % в сутки. В сернокислотных растворах, в которых церий ( ГУ) находится в виде прочных сульфатных комплексов, восстановление церия ( 1У) до церия ( Ш) при хранении на свету практически не наблюдается. [28]
Например, при определении иодид-ионов добавляют анализируемый раствор к раствору, содержащему избыток мышьяковистой кислоты, а затем вводят небольшое количествд сульфата церия ( IV) и измеряют концентрацию церия ( IV) через различные промежутки времени. Этот метод используют, например, для определения содержания иода в солях; в этом случае оценивают степень восстановления церия ( IV) через строго определенные промежутки времени. Было замечено, что очень низкие концентрации иодид-иона оказывают каталитическое действие только в присутствии хлорид-ионов. [29]
Величина выхода восстановления четырехвалентного церия, отвечающего этой пунктирной кривой, примерно на 15 % больше, чем для кривой 1, Увеличение выхода могло произойти в результате увеличения поглощения f - излу-чения. При наличии платины - [ - излучение, поглощенное платиной, могло частично трансформироваться в электроны и этим увеличить выход восстановления церия. Весьма вероятно, что этот эффект связан с уменьшением перенапряжения выделения кислорода на платине при воздействии на нее излучения, что, как уже рассматривалось выше, должно привести к сдвигу равновесия в системе в сторону образования трехвалентного церия. Снижение перенапряжения может быть вызвано действием излучения на окисный слой на платине, аналогично изученному одним из нас [9] действию оптического излучения на аноднополяризованный платиновый электрод. Изучение действия радиоактивного излучения на окисные слои на металлах, служащих электродами, представляет несомненный интерес и является предметом дальнейшего исследования. [30]
Страницы: 1 2 3