Химическое восстановление
Cтраница 1
Химическое восстановление гидразином используется для нанесения катализаторов, в частности палладия и его сплавов, на носители. В работе [267] были получены дисперсные сплавы Pd-Cu, Pd-Ag и Pd-Аи на активном угле. Предварительно уголь пропитывают раствором, содержащим комплексное соединение палладия Na2 [ Pd ( NO2) 4 ] и ионы меди, золота или серебра. Восстановление проводят путем внесения угля, пропитанного раствором солей, в кипящую смесь 25 % - ного аммиака и 15 % - ного гидразин-гидрата равных объемов. Затем катализатор промывают водой и этиловым спиртом и сушат в токе воздуха. [1]
Химическое восстановление в настоящее время широко используют для осаждения никеля или меди в качестве первой стадии электроосаждения на пластинки, особенно такие, как акрилонитрил - бутадиен - стирол, и в меньшей степени полипропилен. Пластик сначала травят в сильной смеси хромовой и серной кислот, сенсибилизируют в растворе двухлористого олова, а затем активируют в палладиевой или серебряной ванне. [2]
Химическое восстановление водородом применяется в качестве метода обесцвечивания окрашенных сточных вод предприятий текстильной промышленности. [3]
Химическое восстановление никеля является автокаталитической реакцией, так как металл, образовавшийся в результате химического восстановления из раствора, катализирует дальнейшую реакцию восстановления этого же металла. Но для начального периода восстановления металла необходимо, чтобы покрываемая поверхность имела каталитические свойства, которые создаются в результате выполнения операции, называемой активированием. Активирование заключается в том, что на обрабатываемую поверхность химическим путем наносят чрезвычайно малые количества металлов, являющихся катализаторами реакции химического восстановления никеля. Такими катализаторами являются коллоидные частицы или малорастворимые соединения палладия, платины, золота, серебра. [4]
 |
Ацетиленовое соединение, которое дает при гидрировании. [5] |
Химическое восстановление диалкилацетиленов натрием в жидком аммиаке в присутствии доноров водорода, таких, как вода или спирт, приводит к транс-олефинам. Точный ход такой реакции не ясен. [6]
Влажное химическое восстановление окислов может быть часто выполнено с минимальными дополнительными затратами на оборудование. Окислы коррозионно-стойкой стали могут быть удалены путем погружения в раствор 50 % - ной по. К по крайней мере на одну минуту с последующим погружением в раствор, состоящий из серной и соляной кислот, при комнатной температуре. Удаление окислов коррозионно-стойкой стали может быть объединено с проведением процесса пассивации. Окислы меди и алюминия могут быть удалены путем погружения медных или алюминиевых частей в раствор, дихлората натрия ( 15 - 45 кг / м3) и серной кислоты ( 4 - 7 % - ной концентрации по объему) при комнатной температуре на 5 - 30 мин. За процессом влажной химической очистки от окислов обычно следует по крайней мере двухминутное промывание деталей водопроводной водой для удаления остатков химикатов. Сразу же после водной промывки детали следует высушить следующим образом: 1) принудительная сушка путем обдувания внутренней поверхности чистым воздухом; 2) промывка безводным изопропиловым спиртом и 3) принудительная сушка в струе чистого сухого азота, подогретого до 70 С. [7]
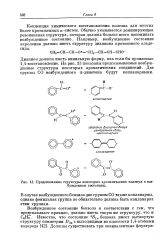 |
Предсказанные структуры некоторых ароматических молекул в возбужденном состоянии. [8] |
Концепция химического восстановления полезна для многих более протяженных я-систем. Обычно указывается доминирующая резонансная структура, которая должна больше всего напоминать возбужденное состояние. Например, возбужденное состояние акролеина должно иметь структуру дианиона кретонового альдегида. [9]
Метод химического восстановления стойких к биохимическому окислению азо - и нитрокрасителей, содержащихся в сточных водах текстильной промышленности, разработан в ЛИСИ. Химизм процесса аналогичен описанному. [10]
Методом химического восстановления получают покрытия толщиной до 30 мкм и более. [11]
Вместо химического восстановления предлагается использовать электрохимическое, однако исходным продуктом Б этом случае будет не хлорат, а двуокись хлора. [12]
Методами химического восстановления из водных растворов могут быть нанесены на металлы и чисто металлические слои из благородных металлов - палладия, платины, золота, серебра, а также меди. Известны некоторые варианты химического осаждения олоаа, свинца, сурьмы, мышьяка. Синтез хромовых покрытий связан с большими трудностями, которые еще не полностью преодолены. [13]
Метод химического восстановления с последующей гальванизацией не требует использования дорогостоящего оборудования, сравнительно прост, дает возможность получать не только однослойные, но и многослойные покрытия. По времени процесс металлизации занимает 60 - 150 мин. [14]
Метод химического восстановления по своему механизму существенно отличается от иммерсионного метода покрытия, который не требует присутствия восстановителя в растворе и при котором электроны на восстановление поступают от металла основы, поскольку последний является более электроотрицательным, чем металл покрытия. Иммерсионное осаждение прекращается, как только основа полностью покрывается осаждающимся металлом. Метод химического восстановления не имеет предела ( во всяком случае теоретического) в отношении толщины образующегося осадка. [15]
Страницы: 1 2 3 4