Химическое восстановление
Cтраница 3
Во многих случаях химическое восстановление проводят в две стадии. [31]
Промышленная реализация процесса химического восстановления во многом определяется особенностями конструкции установок и линий. [32]
На каталитический процесс химического восстановления влияют все компоненты водного раствора. Реагирующие вещества поступают на катализатор диффузией и адсорбируются. Адсорбированные ионы водорода или гидроксила взаимодействуют с буферными соединениями раствора, как бы высвобождая молекулу воды для взаимодействия с восстановителем. [33]
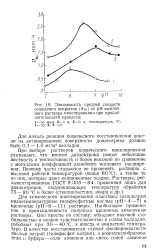 |
Зависимость средней скорости осаждения покрытия ( т от рН аммиачного раствора никелирования при продолжительности процесса. [34] |
Для начала реакции химического восстановления никеля на активированной поверхности диэлектрика должно быть 0 1 - 1 0 мг / м2 палладия. [35]
В отличие от химического восстановления сульфонной функции ( см. раздел VI - Б этой главы) восстановление сульфонов полярографическим методом можно использовать для количественного анализа. Левин и Шестов194 исследовали полярографическое восстановление дифенилсульфона в 50 % - ном этаноле на фоне 0 05 М раствора йодистого тетраэтил-аммония. Сульфон дает волну при потенциале - 2 1 в, при этом наблюдается линейная зависимость высоты волны от концентрации. Присутствие сульфокислот не влияет на результаты анализа. Полярографическое поведение сульфоксидной функции еще до конца не выяснено. Однако Бауэре и Рассел 193 представили данные о восстановлении метилфенил - и дифенил-сульфоксидов. [36]
Медные пленки получают химическим восстановлением фенилгидра-зином в щелочном растворе. Особое развитие для точных работ получило катодное распыление металлов в вакууме; так получают пленки алюминия, серебра, золота, цинка и меди. [37]
При осаждении покрытий химическим восстановлением переход от простых по конфигурации деталей к сложным дополнительных затрат не требует. [38]
Такое явление называется химическим восстановлением рутиловой керамики и связано, очевидно, с уходом части атомов кислорода из испытуемого образца. [39]
Следует отметить, что химическое восстановление протекает глубже и в этом отношении может иметь некоторые преимущества перед электрохимическим. [40]
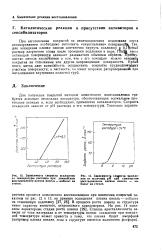 |
Зависимость скорости осаждения [ IMAGE ] Зависимость скорости осажде. [41] |
Для получения покрытий методом химического восстановления требуется довольно несложная аппаратура, обеспечивающая нормальное протекание реакции и, если необходимо, применение катализаторов. Скорость осаждения зависит от рН раствора и его температуры. [42]
К настоящему времени метод химического восстановления используют при осаждении никеля, кобальта, железа, палладия, платины, меди, золота, серебра, родия, рутения и некоторых сплавов на основе этих металлов. Легирующими компонентами этих сплазов являются как каталитически активные металлы, так и металлы, в индивидуальном состоянии неактивные, например, вольфрам, молибден, марганец. [43]
Как известно, методом химического восстановления можно получить покрытия на поверхности, которая катализирует этот процесс. Катализаторами химического палладирования служат металлы восьмой группы, золото, серебро, вольфрам, молибден, а также некоторые полупроводниковые материалы. [44]
Допускается возможность подчинения процесса химического восстановления закономерностям течения сопряженных реакций; при этом несовпадение величин токов и значений потенциалов ( соответственно, резкое снижение коэффициента использования иона ВН4 -) было отнесено за счет особых электрокаталитических свойств сплава Ni-В, на котором скорость восстановления никеля затруднена, а реакция выделения На ускорена. [45]
Страницы: 1 2 3 4