Химическое восстановление
Cтраница 2
Растворы химического восстановления для нанесения покрытия на медь и никель состоят из водных растворов солей тех же металлов. Щелочные растворы используются как для меди, так и для никеля. Для никеля приемлемы также кислотные растворы. [16]
Реакция химического восстановления никеля может идти в кислой и щелочной средах, но широкое промышленное применение находят преимущественно кислые растворы. [17]
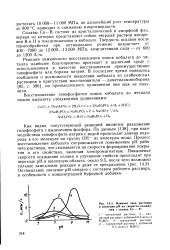 |
Влияние типа раствора и значения рН на скорость осаждения и сплава Со - Р. [18] |
Реакция химического восстановления ионов кобальта до металла наиболее благоприятно протекает в щелочной среде с использованием в качестве восстановителя преимущественно гипофосфита или борана натрия. В последнее время появились сообщения о возможности выделения кобальта из слабокислых растворов в присутствии восстановителя - диметиламиноборана [ 85, с. [19]
Полученный химическим восстановлением никель-фосфорный слой имеет зеркальный блеск с желтоватым оттенком, причем у покрытий, полученных из кислых ванн ( особенно с янтарнокислым натрием или с яблочной кислотой), эта желтизна выделяется сильнее, чем у покрытий из щелочных ванн. Удельный вес Ni - Р покрытий, полученных из кислого раствора, составляет 7 95 - 8 05 г / см3; коэффициент линейного термического расширения 13 - 10 - 6 С; теплопроводность, рассчитанная по данным электропроводности, 0 010 - 0 0135 кал / см - с - С. [20]
Получаемые химическим восстановлением металлопокрытия могут быть использованы для следующих основных целей: повышения износостойкости новых и восстановления работоспособности изношенных деталей, защиты изделий от коррозионных поражений, создания подслоя под пайку % и отражательных поверхностей ( зеркал) для приборов, придания изделиям товарного вида. [21]
При химическом восстановлении осаждение происходит с помощь восстанавливающего агента, который вводят в раствор. [22]
При химическом восстановлении старые напильники очищают в соляной кислоте, обезжиривают кипячением в водном растворе едкого натра и травят в растворе азотной и серной кислот. [23]
При химическом восстановлении в качестве восстановителя чаще всего применяют уголь или окись углерода. [24]
При химическом восстановлении в качестве восстановителя чаще всего применяют уголь или окись углерода. Таким способом получают железо ( в доменном процессе), водород и многие цветные металлы ( олово, свинец, цинк и пр. [25]
При химическом восстановлении нитроксилов в большинстве случаев необходимо присутствие не только донора электронов, но и донора протонов. Этим объясняется устойчивость нитроксилов. С последними нитроксилы взаимодействуют при повышенной температуре в растворителях, способствующих переносу электронов. [26]
 |
Входы и выходы стандартной линии гальваностегии. [27] |
Покрытие методом химического восстановления связано с нанесением металла без электричества. Нанесение покрытий из меди или никеля этим методом используется при изготовлении печатных плат. [28]
Исследование процесса химического восстановления магнитных сплавов Ni-Fe - Р на лавсан. [29]
Данные по электрохимическому и химическому восстановлению нитроксилов позволяют считать, что сила их как окислителей, при отсутствии сильных донорных или акцепторных заместителей, возрастает в ряду ( грет - С дН М - О - - моноциклическиебицикли-ческие. [30]
Страницы: 1 2 3 4