Время - титрование
Cтраница 1
Время титрования линейно зависит от количества таллия в пределах от 0 01 до 0 1 ммоль. Определению таллия не мешают цинк, кадмий и висмут, мешают ртуть и серебро. [1]
Время титрования примесей 15 - 20 мин, температура не должна превышать 25 С. Слабо-коричневый цвет шихты свидетельствует об отсутствии микропримесей. Перед полимеризатором она смешивается с раствором катализатора, который готовится смешением растворов литийорга-нического соединения и полярной добавки, сближающей константы сополимеризации бутадиена и стирола в гексановой фракции. [2]
Время одиночного титрования по индикатору составляет 8 - 10 мин. [3]
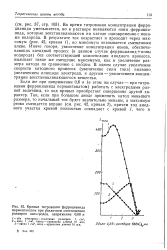 |
Кривые титрования ферроцианида перманганатом при различном соотношении размеров электродов, напряжение 0 60 в. [4] |
Во время титрования концентрация ферро-цианида уменьшается, но в растворе появляются ионы феррициа-нида, которые восстанавливаются на катоде одновременно с ионами водорода. В результате ток возрастает и проходит через максимум ( рис. 42, кривая /), но максимум оказывается смещенным влево. Иначе говоря, увеличение концентрации ионов, обеспечивающих катодный процесс ( в данном случае феррицианид ионы водорода) без соответствующей компенсации анодного процесса, вызывает такое же смещение максимума, как и увеличение размера катода по сравнению с анодом. В одном случае увеличение скорости катодного процесса ( увеличение силы тока) вызвано, увеличением площади электрода, в другом - увеличением концентрации восстанавливающегося вещества. [5]
Во время титрования содержание абсорбера непрерывно перемешивают, затягивая жидкость ртом или резиновой грушей. [6]
Во время титрования часть двуокиси углерода может улетучиваться. Поэтому рекомендуется проводить предварительное титрование. Определив примерно необходимое количество едкого натра, при втором титровании почти все это количество приливают сразу и только потом титруют по каплям до конечной точки. При титровании двуокиси углерода используют свидетель, что облегчает установление точки эквивалентности. [7]
Во время титрования кран 10 должен быть открыт. [8]
Во время титрования содержимое колб энергично взбал-тыванот для лучшего контакта иода с водным раствором тиосульфата натрия. [9]
Во время титрования измеряют оптическую плотность, растворов; вследствие образования осадков оксихинолината или, фталата алюминия поглощение растворов возрастает, достигая максимума в эквивалентной точке. [10]
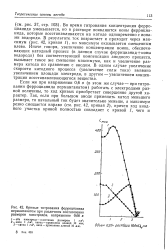 |
Кривые титрования ферроцианида перманганатом при различном соотношении размеров электродов, напряжение 0 60 в. [11] |
Во время титрования концентрация ферро-цианида уменьшается, но в растворе появляются ионы феррициа-нида, которые восстанавливаются на катоде одновременно с ионами водорода. В результате, ток возрастает и проходит через максимум ( рис. 42, кривая 1), но максимум оказывается смещенным влево. Иначе говоря, увеличение концентрации ионов, обеспечивающих катодный процесс ( в данном случае феррицианид ионы водорода) без соответствующей компенсации анодного процесса, вызывает такое же смещение максимума, как и увеличение размера катода по сравнению с анодом. В одном случае увеличение скорости катодного процесса ( увеличение силы тока) вызвано увеличением площади электрода, в другом - увеличением концентрации восстанавливающегося вещества. [12]
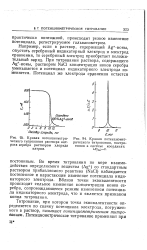 |
Кривая потенциометри-ческого титрования раствора нитрата серебра раствором хлорида натрия.| Кривая потенциомет-рического титрования, построенная в системе координат. [13] |
Во время титрования по мере взаимодействия определяемого вещества ( Ag) со стандартным раствором прибавляемого реактива ( NaCl) наблюдается постепенное и нарастающее изменение потенциала индикаторного электрода. Вблизи точки эквивалентности происходит сильное изменение концентрации ионов серебра, сопровождающееся резким изменением потенциала индикаторного электрода, что и является признаком конца титрования. [14]
 |
Приспособление для колориметрического титрования. [15] |
Страницы: 1 2 3 4