Интенсивность - хемилюминесценция
Cтраница 1
 |
Изменение периода индукции и скорости поглощения кислорода в зависимости от концентрации ФЭС ( температура 200 С. [1] |
Интенсивность хемилюминесценции пропорциональна скорости рекомбинации свободных радикалов, поэтому факторы, влияющие на концентрацию свободных радикалов ( температура, ингибиторы и др.), должны изменять и интенсивность свечения. [2]
Интенсивность хемилюминесценции люминола ( 5-аминодиок-си - 2 3-фталазиндион - 1 4) или люцигенина ( 10 10 -диметил - 9 9 -ди-акридиндинитрат), сопровождающей реакции окисления перекисью водорода, зависит от количества различных неорганических веществ в растворе, которые действуют либо в качестве катализаторов, либо как ингибиторы. [3]
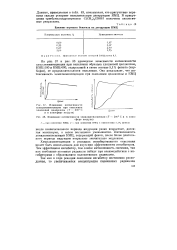 |
Влияние перекиси бензоила на деструкцию КМЦ.| Изменение интенсивности.| Изменение интенсивности хемилюминесценции ( Т - 2009 Сив атмосфере воздуха. [4] |
Интенсивность хемилюминесценции КМЦ, содержащей фенол, после более длительного периода индукции возрастает значительно медленнее. [5]
В реакциях окисления интенсивность хемилюминесценции в системах, содержащих один сорт перекисных радикалов, характеризует их относительную концентрацию. Оценим чувствительность хемилюминесцентного метода обнаружения перекисных радикалов. В присутствии активатора величина светового сигнала, например в реакции окисления этилбензола, в несколько раз превосходит шум при а 4 10 - п - 10 - 12 молъ / л-сек. Отсюда видно, что хемилюминесцентный метод обладает очень высокой чувствительностью. [6]
Таким образом, интенсивность хемилюминесценции пропорциональна концентрации инициатора и связана с температурой арре-ниусовской зависимостью. [7]
Таким образом, интенсивность хемилюминесценции пропорциональна концентрации инициатора и связана с температурой аррениусовской зависимостью. [8]
 |
Температурная зависимость константы скорости рекомбинации переписных радикалов октена-1, ( 1 и нонена-1 ( 2. [9] |
Для других исследованных углеводородов интенсивность хемилюминесценции после подачи кислорода в реакционную систему не описывается линейной функцией от времени, что не позволяет определить константу скорости рекомбинации радикалов вышеприведенным методом. [10]
Таким образом, изменение интенсивности хемилюминесценции при изменении состава окисляющейся смеси определяется кинетическими параметрами Ф и г) и двумя хемилюминесцентными параметрами ifi2и Y22 - Значения параметров Ф иг з можно найти по даннымтабл. Параметру определяется из измерений интенсивности хемилюминесценции чистых кумола и этилбензола. Как видно из рисунка, полученные экспериментальные значения интенсивности хорошо согласуются с теоретической кривой, что количественно подтверждает предложенный механизм изменения интенсивности хемилюминесценции. [11]
Было показано, что как интенсивность хемилюминесценции, так и начальная скорость распада гидроперекиси пропорциональны концентрации гидроперекиси и катализатора. [12]
Уравнение (V.1) показывает, что интенсивность хемилюминесценции непосредственно связана со скоростью реакции, в которой образуется возбужденная частица. Таким образом, измерение интенсивности свечения и ее зависимости от температуры дает сведения о кинетике и механизме реакции. Изучение кинетики реакции можно проводить различными методами: 1) измеряют изменение во времени интенсивности хемилюминесценции изучаемой реакции; 2) добавляют в систему вещество, выход свечения которого велик, и измеряют его хемилюминесценцию, возникающую за счет передачи энергии; при этом изучаемая реакция может не сопровождаться хемилюминесценцией; 3) добавляют в систему хорошо лю-минесцирующее вещество, которое может вступать в хемилюминес-центную реакцию с одним из компонентов системы, например с продуктом; изучаемая реакция при этом также может не сопровождаться хемилюминесценцией. [13]
Для изучения влияния этих соединений на интенсивность хемилюминесценции выбрана реакция окисления этилбензола воздухом. Для повышения растворимости антиокислителей добавлялась уксусная кислота ( 40 объемн. [14]
Таким образом согласно указанному соотношению, интенсивность хемилюминесценции пропорциональна концентрации и экспоненциально зависит от величины, обратной температуре. При этом температурным коэффициентом является энергия активации. Постоянство интенсивности определяется величиной ko, которая для невысоких температур является весьма малой величиной, и временной множитель будет близок к единице. В случае повышенных температур интенсивность должна падать по экспоненциальному закону. [15]
Страницы: 1 2 3 4