Интенсивность - хемилюминесценция
Cтраница 3
При более высоких температурах концентрация ингибитора убывает, и интенсивность хемилюминесценции /, согласно уравнению (V.5), также падает в ходе опыта по экспоненциальному закону. [31]
Добавление FeSO4 в количестве 10 - 4 М усиливает интенсивность хемилюминесценции и увеличивает скорость ее затухания. Влияние ионов Fe2 на ХЛ обусловлено их каталитическим действием на распад Н2О2 по известной схеме Габера-Вейса 44 и реакцией образующихся активных кислородсодержащих радикалов с полимером. [32]
 |
Установка для изучения хеми.| Зависимость интенсивности хемилюминесценции. [33] |
При более высоких температурах концентрация ингибитора убывает, и интенсивность хемилюминесценции /, согласно уравнению (V.5), также падает в ходе опыта по экспоненциальному закону. [34]
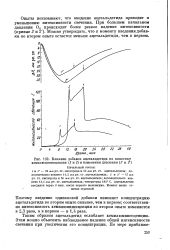
Как видно из рис. 147, участок резкого изменения интенсивности хемилюминесценции занимает всего несколько минут. За это время состав смеси и, в частности, концентрация ацетальдегида заметно не изменяются, что и позволяет использовать уравнение Штерна - Фольмера, условием применения которого является постоянство скорости образования возбужденных частиц. [35]
Добавление кислорода, как правило, увеличивает в этих случаях интенсивность хемилюминесценции растворов, так как оно приводит к появлению перекисных радикалов. [36]
Применение ее основано на зависимости между концентрацией определяемого вещества и интенсивностью хемилюминесценции. Используют жидкофазные реакции окисления хемилюминесцентных индикаторов перекисью водорода, хлором, феррицианидом и другими окислителями. [37]
Поскольку атомы или радикалы возникают в этих системах в больших концентрациях, интенсивность хемилюминесценции высока, н ее наблюдение обычно не представляет затруднений. В газовой фазе возможно изучение хемилюминесценции в инфракрасной области, соответствующей колебательному возбуждению. Такое свечение наблюдается, например, при взаимодействии атомов Н с N0, С12, Br2, NOC1, атомов N с NO, при разряде в молекулярном азоте. [38]
Поскольку атомы или радикалы возникают в этих системах в больших концентрациях, интенсивность хемилюминесценции высока, и ее наблюдение обычно не представляет затруднений. В газовой фазе возможно изучение хемилюминесценции в инфракрасной области, соответствующей колебательному возбуждению. Такое свечение наблюдается, например, при взаимодействии атомов Н с NO, С12, Вг2, NOC1, атомов N с NO, при разряде в молекулярном азоте. [39]
Использование выражений (V.17) - (V.20) открывает возможность определения кинетических параметров по измерениям интенсивности хемилюминесценции. [40]
Превращение углеводородных радикалов в перекисные по реакции с кислородом приводит к резкому усилению интенсивности хемилюминесценции. [41]
Применение хемилюминесценции для указанных целей основано на корреляции между концентрацией определяемого вещества и интенсивностью хемилюминесценции. Первый макет газоанализатора на основе хемилюминесценции появился совсем недавно ( в 1960 г.) [7], в дальнейшем работы в этом направлении получили особенно большое развитие в связи с их актуальностью. [42]
При введении ингибитора в окисляющийся углеводород скорость реакций RO2 - RO2 - уменьшается, поэтому интенсивность хемилюминесценции снижается. [43]
С экспериментальной точки зрения использование любого из описанных методов исследования сводится либо к изучению зависимости интенсивности хемилюминесценции от концентрации ингибитора, либо к получению серии кинетических кривых изменения интенсивности свечения. [44]
 |
Влияние добавок ацетальдегида на кинетику хемилюминесценции ( 1 и 2 и изменения давления ( Г и 2. [45] |
Страницы: 1 2 3 4