Изученный интервал - концентрация
Cтраница 1
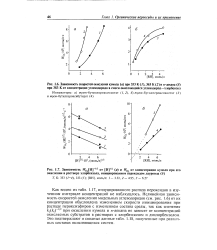
Изученный интервал концентраций 5 - ю 6 - 2 - ю - моль / см, что отвечает интервалу давлений 0 8 - 300 атм. [1]
В изученном интервале концентраций ( 0 5 - 0 025 моль / л) химические сдвиги описанных сигналов практически постоянны. При добавлении в раствор кислородсодержащих акцепторов протона ( ( C2Hs) 2O, ( CH3) 2SO, СНзСООС Нз, HGON ( CH3) 2, ( С4Н9) зРО) сигнал протона СН-группы сильно смещается в сторону слабого поля. [2]
Следовательно, изученный интервал концентраций следует подразделить на два участка: от 3 - 10 2 до 10 - 5 г-ат. [3]
Следовательно, изученный интервал концентраций следует подразделить на два участка: от 3 10 - 2 до 10 - 5 г-ат. Возможное объяснение увеличения адсорбции иттрия при уменьшении его концентрации в растворе может быть сведено к двум обстоятельствам: 1) при уменьшении концентрации иттрия происходит переход из области насыщения фильтра в область линейной зависимости величины адсорбции от концентрации, поэтому процент адсорбции вначале растет, а затем вплоть до концентрации иттрия 10 - п г-ат. [4]
Фактически в изученном интервале концентраций молекулярный вес не зависел от типа и концентрации катализатора. [5]
Ка практически постоянны в изученном интервале концентраций. [6]
Отсутствие оптимума кислотности ( в изученном интервале концентраций) при гетерогенном нитровании объясняют иногда тем, что концентрация активной формы нитруемого соединения в кислотном слое растет за счет растворения быстрее, чем происходит падение ее из-за протонирования серной кислотой. Такой подход, однако, предполагает, что либо степень ионизации насыщенных растворов АгН в серной кислоте уменьшается с ростом ее концентрации, либо максимум скорости сдвинут в область более высоких концентраций HaSO; это нуждается в доказательствах, и в первую очередь необходимо изучение зависимости скорости нитрования в гетерогенных условиях более концентрированными кислотами. Другое возможное объяснение заключается в том, что в условиях избытка основания ( АгН) кислотность среды при гетерогенном нитровании в крепких смесях не изменяется и, следовательно, не может лроявиться ее влияние на активность нитрующего агента. [7]
Было показано, что в изученном интервале концентраций скорость пропорциональна произведению концентраций обоих компонентов. Скорость реакции имеет резкий максимум при рН, равном 10 ( рис. 7); она падает при увеличении или уменьшении величины рН, Эго свидетельствует о невозможности реакции между молекулами одного реагента и ионами другого. [8]
Водные растворы фосфорной кислоты в изученном интервале концентраций ( дои98 % Н3РО4) при нагревании выделяют в газовую фазу только водяной пар, следовательно теоретически фосфорная кислота может быть выпарена до очень высоких концентраций. [9]
В системе HCOOLi - НСООН-Н2О при 25 С в изученном интервале концентраций НСООН в твердой фазе выделяется только моногидрат состава HCOOLi - H2O, что. [10]
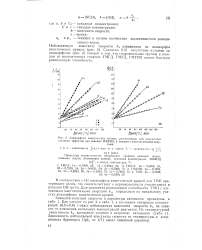 |
Анаморфозы кинетических кривых, рассчитанные для полученных тепловых эффектов при реакции МХФИЦ в диглиме с многоатомными спир. [11] |
Как следует из рис. 2 и табл. 1, в изученном интервале концентраций ( 0 5 - - 0 8) r - экв / л наблюдаемая константа скорости ka не зависит от изменения начальных концентраций реагентов. Зависимость наблюдаемой константы скорости от температуры в координатах Аррениуса ( gka от 1 / Г) имеет линейный характер. [12]
Как видно из табл. 1.17, индуцированного распада пероксидов в изученном интервале концентраций не наблюдалось. Это подтверждают и сводные данные табл. 1.18, полученные при различных составах окисляющихся систем. [14]
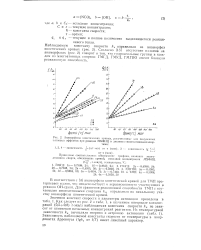 |
Анаморфозы кинетических кривых, рассчитанные для полученных тепловых эффектов при реакции МХФИЦ в диглиме с многоатомными спиртами. [15] |
Страницы: 1 2 3 4