Изученный интервал - концентрация
Cтраница 2
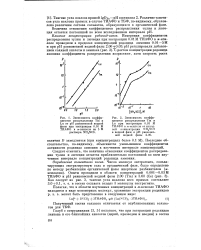
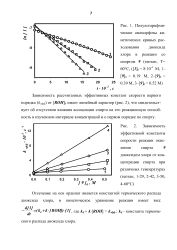
Как следует из рис. 2 и табл. 1, в изученном интервале концентраций ( 0 5 - 0 8) г-экв / л наблюдаемая константа скорости kK не зависит от изменения начальных концентраций реагентов. Зависимость наблюдаемой константы скорости от температуры в координатах Аррениуса ( gkH от 1 / Т) имеет линейный характер. [16]
Прямолинейная зависимость скорости реакции от количества катализатора ( Скт) в изученном интервале концентраций ( рис. 2) указывает на первый порядок реакции по катализатору. [17]
Рентгеноанализ показал, что все полученные образцы обладают структурой перовскита в изученном интервале концентраций ( до 30 мол. При этом вблизи чистого титаната бария наблюдалась тетрагональная модификация твердых растворов, а при увеличении концентрации вторых компонентов - кубическая. Концентрационные зависимости параметров элементарной ячейки и Тс на частоте 1 5 Мгц приведены на рис. I, а, б, в. Как видно из рисунка, для всех добавок характерно нелинейное изменение Тс от состава. [18]
Последнее обстоятельство, по-видимому, объясняется уменьшением коэффициентов активности роданида аммония в изученном интервале концентраций. [20]
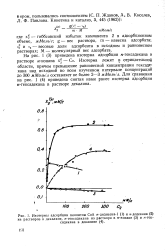 |
Изотермы адсорбции цеолитом СаА н-додецена-1 ( 1 и н-додекана ( 2 из растворов в декалине, и-гексадекана из раствора в н-нонане ( 3 и н-гексадекана в декалине ( 4. [21] |
Изотерма лежит в отрицательной области, причем превышение равновесной концентрации гексаде-кана над исходной во всем изученном интервале концентраций до 300 м Моль. Для сравнения на рис. 1 ( 4) приведена снятая нами ранее изотерма адсорбции н-гексадекана в растворе декалина. [22]
Как следует из рисунка, технеций и рений экстрагируются с высокими коэффициентами распределения во всем изученном интервале концентраций кислоты, в то время как молибден экстрагируется значительно хуже. Это, по-видимому, может быть использовано для разработки метода экстракционного отделения технеция и рения от молибдена. [23]
Следует отметить, что величина отношения коэффициентов распределения тулия и лютеция остается приблизительно постоянной во всем изученном интервале концентраций роданида аммония. [24]
Средние значения Р и Ка приводятся только для тех случаев, когда величины Р я Ка практически постоянны в изученном интервале концентраций. [25]
ROH Q имеет линейный характер ( рис. 2), что свидетельствует об отсутствии влияния ассоциации спирта на его реакционную способность в изученном интервале концентраций и о первом порядке по спирту. [27]
Строят график зави - - симости D-с ( моль / л) и находят коэффициент наклона А полученной прямой, равный отношению D / c для изученного интервала концентраций. [28]
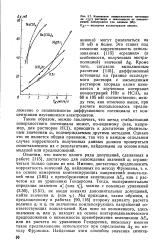 |
Изменения поверхностного потенциала ( ДХ раствора в зависимости от концентрации электролита ( по данным. Сд - - молярная концентрация аниона. [29] |
Это ставит под сомнение коррективность использованных [115] средних ( в особенности, полученных экстраполяцией) значений АХ - Кроме того, согласно выполненным расчетам [115], диффузионный потенциал на границе исследуемого раствора с насыщенным раствором хлорида калия изменяется в изученном интервале концентраций НВг и НС1О4 на 60 и 105 мВ соответственно; между тем, как отмечено выше, при расчете использовалось предположение о независимости диффузионного потенциала от концентрации изучавшихся электролитов. [30]
Страницы: 1 2 3 4