Изученный интервал - концентрация
Cтраница 4
Если же данных о К и а, в литературе нет, то для изучаемой системы сравнительно несложно найти их специальными опытами. Поскольку воспроизводимость результатов, получаемых при изучении ионообменных процессов, как правило, невелика ( из-за неоднородности структуры ионообменника, трудности стандартизации размера его зерен и других причин), обычно эту задачу не усложняют учетом коэффициентов активности, а устанавливают величину концентрационной константы обмена, приняв для изучаемого процесса какой-то определенный механизм. Если опытные данные, подставленные в соответствующую расчетную формулу, не дают стабильной константы, следует сделать вывод, что принятый для объяснения механизм неудовлетворительно описывает процесс. Если удается получить константу, достаточно стабильную в изученном интервале концентраций, ее используют для расчетов таких систем с концентрациями, естественно, не выходящими за пределы указанного интервала. [46]
Таким образом / наблюдаются некоторые чередующиеся концентрационные интервалы, некоторых структурные / особенн оет и границ проявляют себя в кинетических свойствах. Полученные результаты показывают в частности, что выводы, сделанные в работах [8, 14, 48], а также в статье, О. Согласно им с увеличением концентрации примеси энергия активации миграции ( и подвижность) обычных границ изменяется достаточно резко, тогда как для специальных границ она остается практически неизменной во всем изученном интервале концентраций. [47]
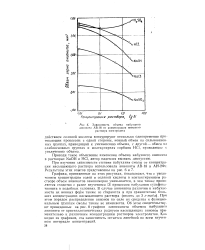 |
Зависимость объема набухшего. [48] |
Графики, приведенные на этих рисунках, показывают, что с увеличением концентрации солей и соляной кислоты в контактирующем растворе объем анионитов закономерно уменьшается, в чем также проявляется сходство с ранее изученным [ 31 процессом набухания сульфока-тионита в подобных условиях. В случае анионитов различия в набухае-мости их ионных форм также не стираются и при сравнительно больших концентрациях насыщающего раствора ( вплоть до 3 г-экв. При этом порядок распределения анионов по силе их сродства к функциональным группам смолы также не изменяется. Об этом свидетельствуют приведенные на рис. 8 графики зависимости объемов набухшего анионита от кристаллохимических радиусов насыщающих анионов применительно к различным концентрациям растворов электролитов. Как видно из графиков, эта зависимость остается линейной во всем изученном интервале концентраций. [49]
Страницы: 1 2 3 4