Выделение - льд
Cтраница 3
При охлаждении раствора до криогидратной температуры в осадок будет выпадать только лед, так как вертикаль AWj, проходящая через точку 12 % раствора КС1, пересекает кривую выделения льда и весь хлористый калий остается в растворе. [31]
Обычно, когда золь кремнезема замерзает, выделение льда приводит к увеличению концентрации SiOo, так что образуется гель. Однако в этом случае замерзший золь может быть при последующем нагревании превращен в первоначальное жидкое состояние. Если этот золь концентрировать путем выпаривания и, наконец, высушить, то твердый продукт может быть снова растворен в воде с получением прозрачного устойчивого золя, подобного исходному. Другой замечательной особенностью этого золя является то. [32]
Участок АВ определяет условия равновесия между раствором и льдом. При изменении состава раствора по ветви АВ ( добавлением NaBr) происходит выделение льда с одновременным понижением температуры раствора. [33]
Линия ВК на диаграмме является геометрическим местом фигуративных точек растворов, насыщенных солью ( например точка Мг), а линия ОК-растворов, находящихся в равновесии со льдом. Линия ВК является кривой растворимости соли, а линия ОК отвечает условиям выделения льда в системе соль - вода. Фигуративная точка О изображает чистую воду при температуре замерзания, а точка В - чистую 100 % соль при температуре плавления. [34]
 |
Схема рассольного охлаждения.| Схемы испарителей без затопления и затопленных. [35] |
С экономической точки зрения выбор концентрации ограничен областью, лежащей над линией выделения льда. [36]
Участок АВ определяет условия равновесия между раствором и льдом. При изменении состава раствора по ветви А В ( добавлением NaBr) происходит выделение льда с одновременным понижением температуры раствора. [37]
Линия ВК на диаграмме является геометрическим местом фигуративных точек растворов, насыщенных солью ( например точка Mv), а линия ОК - растворов, находящихся в равновесии со льдом. Линия В К является кривой растворимости соли, а линия ОК отвечает условиям выделения льда в системе соль - вода. Фигуративная точка О изображает чистую воду при температуре замерзания, а точка В - чистую 100 % соль при температуре плавления. [38]
Вода, содержание которой соответствует максимальной гигроскопичности, в почвах с высокой адсорбционной способностью не замерзает и при - 78 С. Присутствие в воде растворенных солей малой концентрации при охлаждении ниже О С приводит к выделению чистого льда и к увеличению концентрации раствора. Раствор высокой концентрации при охлаждении становится перенасыщенным, и из него начинают выделяться кристаллы соли. С, в монтморило-ните при - 70 С еще содержится 7 % незамерзшей воды. [39]
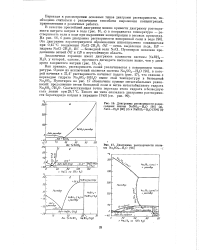 |
Диаграммы растворимости водно-солевых систем NaNOg - H20 ( а, NaCl - Н20 ( б и NaBH4 - Н20 ( в.| Диаграмма растворимости системы Na2S04 - Н20 -. - - I. [40] |
Эта диаграмма характеризуется образованием инконгруэнтно плавящегося при 0 15 С соединения NaCl - 2H20; ОЕ - ветвь выделения льда, ЕВ - гидрата NaCl - 2H20, BC - безводной соли NaCl. Пунктиром показано продолжение ветвей ОЕ и СВ в неустойчивую область. [41]
Чтобы более наглядно представить себе возникающую здесь ситуацию, рассмотрим следующий пример: пусть температура контакта в адсорбере составляет 20 С, а газ осушен до остаточного влагосодержания, отвечающего точке росы по переохлажденной воде, равной - 20 С. Тогда удельное количество W выделяющейся жидкой фазы ( водного раствора гликоля) в зависимости от температуры, абстрагируясь от возможности выделения льда и ( или) гидратной фазы, можно представить схемой ( рис. 4.1), из которой видно, что вблизи температуры t - 20 С имеет место довольно резкое увеличение количества выделяющейся жидкости из газовой фазы. Отметим еще, что для предельного случая нерастворимого в сжатом газе абсорбента эта вторая производная при температуре точки росы обращается в бесконечность. [42]
Наиболее трудным является подбор теплоизоляции, пригодной для эксплуатации при столь низких температурах. Проникание в теплоизоляцию аппаратуры влаги, содержащейся в окружающем воздухе, приводит к ухудшению изоляционных свойств и может служить причиной разрушения стенок аппаратов вследствие выделения льда. Поэтому одним из важнейших требований, которым должна удовлетворять теплоизоляция, является невозможность проникания в нее влаги. Зачастую вся аппаратура помещается в плотный ( по возможности) кожух из древесины или листовой стали, заполненный шлаковой ватой. [43]
Левые кривые показывают выделение льда, а правые-соли. Если рассол NaCl, имеющий 15 весовых частей соли на 100 частей воды при 0, охладить, то до t - - 10 концентрация не изменится, а затем начнется выделение кристаллов льда; состояния остающегося жидкого раствора характеризуются точками, лежащими на кривой выделения льда, и концентрация соли будет увеличиваться до тех пор, пока охлаждаемый раствор не достигнет температуры криогидратной точки, затем весь раствор затвердевает, превращаясь в однородную массу. [44]
На рис. 10.1 точка F характеризует содержание воды ( 100 %), а - точка Н-100 % безводной соли. Линия В / С - геометрическое место фигуративных точек растворов, насыщенных солью В ( например, точка MI), а линия О / С - растворов, находящихся в равновесии со льдом. Линия В / С - кривая растворимости соли, а линия О / С отвечает условиям выделения льда в системе соль - вода. Фигуративная точка О характеризует воду при температуре замерзания, а точка В - чистую соль при температуре плавления. [45]
Страницы: 1 2 3 4