Выделение - льд
Cтраница 4
Аналогично изменится линия насыщения солью С и льдом ( пойдет внутрь призмы и вниз) при добавлении к системе компонента В. Таким образом, может быть получена полная диаграмма растворимости трехкомпонентной системы, где область EiE2HO соответствует растворам, насыщенным солью В; ОЕъРЕъ - растворам, насыщенным солью С; OEiKE - область выделения льда. Линии ОЕ, ОЕ2 и 0.3 совместного выделения двух твердых фаз разграничивают поля насыщения этими твердыми фазами. [46]
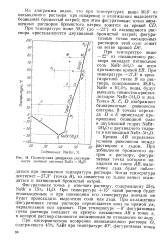 |
Политермная диаграмма растворимости двойной системы NaBr - НзО. [47] |
При температуре ниже - 22 из насыщенного раствора выпадает пятиводная соль NaBr - 5H3O на всем протяжении кривой ЕВ. NaBr и 61 4 % воды, будут выпадать совместно кристаллогидрат NaBr - 5H2O и лед, Точки В, Е, D изображают безвариантные равновесия системы. Кривая АВ определяет условия равновесия между раствором и льдом. При добавлении бромистого натрия к раствору, фигуративная точка которого находится на линии АВ, выделение льда будет наблюдаться при понижении температуры раствора. Когда температура достигнет - 27 3 ( точка В), то совместно со льдом начнет осаждаться и пятиводный бромистый натрий. [48]
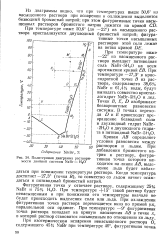 |
Политермная диаграмма растворимости двойной системы NaBr - Н2О. [49] |
При температуре ниже - 22 из насыщенного раствора выпадает пятиводная соль NaBr - 5H2O на всем протяжении кривой ЕВ. При температуре - 27 3 в крио-гидратной точке В из раствора, содержащего 38 6 %, NaBr и 61 4 % воды, будут выпадать совместно кристаллогидрат NaBr - 5H2O и лед. Точки В, Е, D изображают безвариантные равновесия системы. Кривая АВ определяет условия равновесия между раствором и льдом. При добавлении бромистого натрия к раствору, фигуративная точка которого находится на линии АВ, выделение льда будет наблюдаться при понижении температуры раствора. Когда температура, достигнет - 27 3 ( точка В), то совместно со льдом начнет осаждаться и пятиводный бромистый натрий. [50]
Кристаллизация растворов проходит так же, как в металлических расплавах. Любой водный раствор нитрата калия, содержащий го в концентрации ниже 11 62 %, при охлаждении выделяет сначала кристаллы льда. Их выделение начинается при температуре, которая определяется кривой кристаллизации льда. Так, из раствора, содержащего 3 34 % KNO3, выделение кристаллов льда начинается при - 1 0 С. При дальнейшем понижении температуры выделение кристаллов льда продолжается. По мере выделения льда раствор становится более концентрированным. Содержание соли в нем для каждой температуры определяется кривой кристаллизации льда. Для каждого интервала температур количество выделяющегося льда строго определенно. Дальнейшее охлаждение приведет систему в состояние, представляемое криогидратной точкой. При этой температуре ( при дальнейшем отнятии теплоты) остающийся раствор замерзает полностью в виде криогидрата. [51]
Так как растворимость некоторых веществ ( напр, кониина, серно-цериевой соли и др.) уменьшается с повышением температуры ( между известными пределами, см. напр. Так, раствор MnSCH, насыщенный при 70, при дальнейшем нагревании мутится. Начало выделения растворенного вещества при перемене температуры служит легким средством для определения коэффициента растворимости, чем и воспользовался проф. Из этого примера и существа дела ясно, что выделение растворенного тела представляет - некоторую аналогию с выделением льда из растворов. В обоих случаях из однородной ( гомогенной, жидкой) системы раствора образуется ( гетерогенная) система твердого и жидкого вещества. [52]
Так, например, при охлаждении раствора, содержащего 34 2 % азотнокислого серебра, до - 5 6 вода начинает кристаллизоваться, вымерзать. При дальнейшем охлаждении содержание воды в жидкой части раствора уменьшается, а соли - возрастает. Температура плавления или отвердевания любого вещества понижается при растворении в нем другого вещества. Кривая АЕ отражает изменение температуры выделения льда от прибавления азотнокислого серебра. В случае водных растворов солей эвтектическая точка называется криогидратой точкой. При охлаждении раствора, содержащего 47 1 % азотнокислого серебра, ниже температуры, соответствующей этой точке, имеет место переход жидкой фазы в твердую. Выпадающая из раствора твердая фаза, несмотря на постоянство состава, все же отнюдь не является химическим соединением соли и воды. В данном случае это подтверждается тем, что при обработке массы холодным спиртом воду и лед можно извлечь, а кристаллики твердой соли остаются без изменения. Возможность такого разделения льда и азотнокислого серебра указывает на то, что они образуют смесь. В случае окрашенных солей неоднородность может быть обнаружена и путем непосредственного наблюдения под микроскопом. [53]
Страницы: 1 2 3 4