Выделение - перекись - водород
Cтраница 1
 |
Установил для ректификации разбавленных растворов H. O2 ( фр. пат. 563908. [1] |
Выделения перекиси водорода из смеси ее паров с водяными парами можно достигнуть, конечно, и обычной ректификацией. [2]
Так как выделение перекиси водорода из твердых персульфатов оказалось возможным через персульфат калия, необходимо было найти сначала экономичный способ производства этой соли. В качестве исходного материала был выбран персульфат аммонии, легко получающийся электрохимическим путем с хорошим выходом г / о току. [3]
Проверка процесса выделения перекиси водорода из реакционных смесей отгонкой органической части, Отч. [4]
Это обстоятельство затрудняет выделение перекиси водорода, требует обращения в рецикле огромных количеств рабочих растворов, что, в свою очередь, ведет к увеличению расхода дорогостоящего сырья и электроэнергии. Поэтому с первых лет существования антрахинонного метода предпринимаются многочисленные попытки устранить указанный недостаток. [5]
Экстракцию применяют для выделения перекиси водорода из реакционной смеси при получении ее новейшим автоокислительным способом. В этом процессе 2-этилантрахинон каталитически гидрируется в подходящей среде ( нониловом спирте или алкилзамещенных циклогексанола) в соответствующее производное антрагидрохинона. При окислении последнего воздухом получают снова антрахинон и Н2О2 в органическом растворителе. Перекись экстрагируют обессоленной водой в очень крупных экстракторах, чаще всего в колоннах с ситчатыми тарелками или в насадочных колоннах. Экстракт, содержащий около 20 % перекиси водорода, для извлечения следов растворителя экстрагируют каким-либо углеводородом, который удаляют продувкой воздухом. [6]
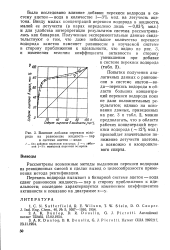 |
Влияние добавки перекиси водорода на равновесие жидкость - пар в системе ацетон - вода. [7] |
Рассмотрены возможные методы выделения перекиси водорода из реакционных смесей и сделан вывод о целесообразности применения метода ректификации. [8]
Предварительная оценка и экспериментальная проверка перечисленных способов выделения перекиси водорода из реакционных смесей указанного состава показала, что наиболее простым, удобным и экономичным является метод ректификации. [9]
Предварительная оценка и экспериментальная проверка перечисленных способов выделения перекиси водорода из реакционных смесей указанного состава показала, что наиболее простым, удобным и экономичным является метод ректификации. [10]
Так как пероксигидраты боратов в водных растворах разлагаются с выделением перекиси водорода, то они оказывают совершенно такое же действие, как и сама Н202 - легко отщепляют кислород, передавая его другим веществам. На этом основано применение перборатов ( пероксигид-ратов боратов) в промышленности в качестве средства для отмывки и отбеливания шерсти, шелка, соломы, слоновой кости и многих других веществ. Обширное применение находят они также и в косметике ( для обесцвечивания волос), а также в качестве дезинфицирующего средства. В смеси с веществами, каталитически разлагающими с выделением 02 пербораты или выделяющуюся при их растворении перекись водорода, их используют для получения кислорода. При работе с пероксигидратами боратов, содержащими более 15 % активного кислорода, необходима осторожность, так как они при трении способны разлагаться со взрывом. [11]
Так как пероксигидраты боратов в водных растворах разлагаются с выделением перекиси водорода, то они оказывают совершенно такое же действие, как и сама Н202, - легко отщепляют кислород, передавая его другим веществам. На этом основано применение перборатов ( пероксигидратов боратов) в промышленности в качестве средства для отмывки ж отбеливания шерсти, шелка, соломы, слоновой кости и многих других веществ. Обширное применение находят они также и в косметике ( для обесцвечивания волос), а также в качестве дезинфицирующего средства. В смеси с веществами, каталитически разлагающими с выделением 02 пербораты или выделяющуюся нри их растворении перекись водорода, жх используют для получения кислорода. При работе с пероксигидратами боратов, содержащими более 15 % активного кислорода, необходима осторожность, так как они при трении способны разлагаться со взрывом. [12]
Так как пероксигидраты боратов в водных растворах разлагаются с выделением перекиси водорода, то они оказывают совершенно такое же действие, как и сама Н202, - легко отщепляют кислород, передавая его другим веществам. На этом основано применение перборатов ( пероксигидратов боратов) в промышленности в качестве средства для отмывки и отбеливания шерсти, шелка, соломы, слоновой кости и многих других веществ. Обширное применение находят они также и в косметике ( для обесцвечивания волос), а также в качестве дезинфицирующего средства. В смеси с веществами, каталитически разлагающими с выделением 02 пербораты или выделяющуюся при их растворении перекись водорода, их используют для получения кислорода. При работе с пероксигидратами боратов, содержащими более 15 % активного кислорода, необходима осторожность, так как они при трении способны разлагаться со взрывом. [13]
С данными опытов Павлова интересно сравнить исследования Клеменца 4 по выделению перекиси водорода при электролизе с тлеющим разрядом, с окислением на аноде и образованием перекиси на катоде. Автором была определена скорость получения перекиси на катоде в растворах сернокислого магния, изучены реакции на границе электролит - газ и электролит - металл и показэ-но различие этих реакций для водорода и кислорода. В более ранней работе Клемсниемг был исследован анодный процесс образования перекиси при наложении переменного тока и выведено уравнение скорости получения перекиси на цинковом аноде. [14]
Соединения, образующиеся в электролизере, подвергаются затем гидролизу с целью выделения перекиси водорода. [15]
Страницы: 1 2 3