Выделение - хром
Cтраница 2
С повышением плотности тока при выделении хрома катодный потенциал изменяется мало, а выход металла по току увеличивается, поэтому электролит имеет очень низкую рассеивающую способность. Кроме того, прекращение выделения металла при низких плотностях тока делает вообще невозможным получение сплошного покрытия на рельефной поверхности. [16]
При плотностях тока, при которых происходит выделение хрома, ультразвук не оказывает существенного влияния на величину катодной поляризации. [17]
Так как с повышением плотности тока при выделении хрома катодный потенциал изменяется мало, а выход металла по току увеличивается, электролит имеет очень низкую рассеивающую способность. Кроме того, отсутствие выделения металла при низких плотностях тока делает вообще невозможным получение сплошного покрытия на рельефной поверхности. В случае хромирования очень рельефных изделий, особенно при нанесении относительно толстого покрытия, применяют профилированные аноды или к углубленным местам ПОДЕЮДЯТ дополнительные аноды. [18]
Так как с повышением плотности тока при выделении хрома катодный потенциал изменяется мало, а выход металла по току увеличивается, электролит имеет очень низкую рассеивающую способность. Кроме того, отсутствие выделения металла при низких плотностях тока делает вообще невозможным получение сплошного покрытия на рельефной поверхности. В случае хромирования очень рельефных изделий, особенно при нанесении относительно толстого покрытия, применяют профилированные аноды или к углубленным местам подводят дополнительные аноды. [19]
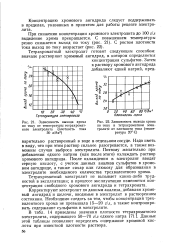 |
Зависимость выхода хрома.| Зависимость выхода хрома. [20] |
При снижении концентрации хромового электролита до 100 г. л выделение хрома прекращается. [21]
За последнее время проводится все большее число исследований по выделению хрома из хромовых руд хлорным методом. Большая разность температур кипения получаемых продуктов хлорирования позволяет получить достаточно чистые от посторонних примесей хлориды хрома. Хлориды хрома могут быть либо использованы для получения металлического хрома путем электролиза в расплавленных или водных средах или непосредственным восстановлением ( например, магнием, водородом), либо переработаны в окись хрома. Процесс осуществляют обычно в шахтных печах. В качестве восстановителя может быть использован каменный уголь, древесный уголь или кокс. [22]
 |
Нормы расхода химикатов на разложение для I м2 поверхности при толщине 1 мкм. [23] |
При расчете норм расхода хромового ангидрида следует к потерям электролита на унос в промывные воды и вентиляцию добавить расход на выделение хрома. [24]
Электролитическое хромирование существенно отличается от других гальванических процессов. Выделение хрома производится из растворов хромовых кислот ( смесь кислот HiCr Qj и HjCrO-i), а не из солей хрома. При этом в растворе обязательно должны присутствовать в небольшом количестве добавки активных анионов ( SOI, StFl -, F -), без которых хром не выделяется из хромовой кислоты. Электролиты, основанные на солях хрома, широко изучаются, но до сих пор не получили промышленного применения. [25]
Остальная часть тока расходуется неэффективно - на выделение водорода. Аналогичное положение наблюдается при выделении хрома из шестввалентных солей: катодный выход хрома по току еще ниже. При получении металлов из расплавленных электролитов, не содержащих ионов водорода, электроэнергия не расходуется на совместное выделение водорода и, следовательно, металл не содержит примесей водорода. Именно поэтому исследователи неоднократно, начиная с начала XX в. [26]
Остальная часть тока расходуется неэффективно - на выделение водорода. Аналогичное положение наблюдается при выделении хрома из шестивалентных содей: катодный выход хрома по току еще ниже. При получении металлов из расплавленных электролитов, не содержащих ионов водорода, электроэнергия не расходуется на совместное выделение водорода и, следовательно, металл не содержит примесей водорода. Именно поэтому исследователи неоднократно, начиная с начала XX в. [27]
При достижении толщины в несколько микрон выделение хрома прекращается. Использование новых электролитов дало возможность проводить осаждение хрома с выходами по току до 25 - 45 % и скоростью 0 8 - 1 6 мкм / мин вне зависимости от времени. [28]
Электролизом кислого водного раствора можно выделить и многие другие металлы ( кобальт, никель, хром, цинк), несмотря на то, что потенциалы их восстановления отрицательны ( см. табл. 16.1) и при электролизе получается водород. В некоторых случаях, например при выделении хрома, действительно, одновременно образуется и водород, который частично поглощается образующимся хромом, в результате чего металл становится пористым. Этот недостаток, а также лишний расход электроэнергии на получение водорода компенсируется тем, что после удаления водорода нагреванием сам хром переходит в другую модификацию, обладающую большей твердостью. В других случаях положение спасает перенапряжение выделения водорода ( см. разд. В частности, если сернокислый раствор не содержит примесей, снижающих высокое перенапряжение выделения водорода, то из него удается осадить цинк ( Е ( Zn2 / Zn) - 0 760 В) без заметного выделения водорода. [29]
Никелевая пластинка вносится в раствор соли трехвалентного хрома. Определите, возможно ли растворение никеля и выделение хрома. [30]
Страницы: 1 2 3 4