Катодное выделение - водород
Cтраница 1
Катодное выделение водорода всегда имеет место при электролизе водных растворов электролитов. Реакция катодного восстановления водорода протекает на некоторых металлах со значительным перенапряжением, существенно превышающим перенапряжение многих других электродных реакций. Величина водородного перенапряжения зависит от многих факторов, и в первую очередь от состава раствора, материала катода и состояния его поверхности, плотности тока и температуры. Рассмотрим возможные пути выделения водорода из кислых и щелочных растворов. [1]
Катодное выделение водорода протекает с большим или меньшим перенапряжением в зависимости от материала электрода, особенно оно велико на ртути. [2]
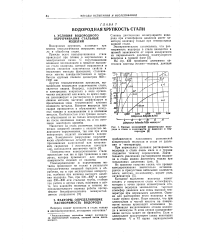 |
Кривые равновесной концентрации водорода в стали в зависимости от давления и температуры. [3] |
Катодное выделение водорода может создать у поверхности стали атмосферу, которая с точки зрения концентрации атомарного водорода эквивалентна тысячам атмосфер давления или очень высокой температуре при нормальном давлении. Однако для растворения этого водорода в металле нужно время. Опыт показал, что при электролизе в чистой кислоте на поверхности катода происходит мгновенная рекомбинация выделяющихся атомов водорода в молекулы. В этом случае наводороживание катода может не произойти. [4]
Процесс катодного выделения водорода на ртути и подобных катодах происходит по механизму замедленный разряд - электрохимическая десорбция. Естественно, что суммарная скорость перехода какого-либо изотопа из раствора в газ определяется не только скоростью его разряда, но и скоростью его электрохимической десорбции. [5]
Реакция катодного выделения водорода также относится к числу сложных многостадийных процессов. [6]
Реакция катодного выделения водорода - сложная двухэлект-ронная реакция, протекающая последовательно через несколько более простых промежуточных стадий. [7]
Процесс катодного выделения водорода на ртути и подобных катодах происходит по механизму замедленный разряд - электрохимическая десорбция. Естественно, что суммарная скорость перехода какого-либо изотопа из раствора в газ определяется не только скоростью его разряда, но и скоростью его электрохимической десорбции. [8]
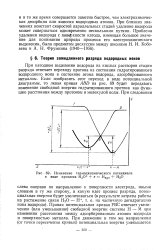 |
Изменение термодинамического потенциала в ходе процесса Н3О е Hagc ЩО. [9] |
При катодном выделении водорода из кислых растворов стадия разряда отвечает переходу протона из состояния гидратированного водородного иона в состояние атома водорода, адсорбированного металлом. [10]
 |
Возможные комбинации стадий. [11] |
Действительный механизм катодного выделения водорода на каждом данном металле удается установить на основании всесторонних экспериментальных исследований и их сопоставления с выводами, вытекающими из теории возникновения различных видов перенапряжения. [12]
В области катодного выделения водорода для большинства металлов - потенциал имеет отрицательное значение. Оно зависит как от общей концентрации электролита, так и от наличия в растворе специфически адсорбирующихся поверхностно-активных ионов. [14]
Однако при катодном выделении водорода из обезжиривающего электролита, так же как и при осаждении тяжелых металлов из цианистых растворов, не может быть достигнут потенциал осаждения калия и натрия, имеющий значение около - 2 92 и - 2 718 в. [15]
Страницы: 1 2 3 4