Катодное выделение - водород
Cтраница 2
В отличие от катодного выделения водорода прямолинейная зависимость г - lg i [ см. уравнение (1.11) ] при анодном выделении кислорода не сохраняется в широком интервале плотностей тока. На поляризационных кривых может наблюдаться несколько прямолинейных участков, причем наклоны их будут разными. [16]
В отличие от катодного выделения водорода прямолинейная зависимость т) - lg i [ см. уравнение (1.11) ] при анодном выделении кислорода не сохраняется в широком интервале плотностей тока. На поляризационных кривых может наблюдаться несколько прямолинейных участков, причем наклоны их будут разными. [17]
В отличие от катодного выделения водорода прямолинейная зависимость г ] - lg i [ см. уравнение (1.11) ] при анодном выделении кислорода не сохраняется в широком интервале плотностей тока. [18]
Реакция Гейровского при катодном выделении водорода заключается в разряде гидратированного или сольватированного иона водорода на уже адсорбированном на поверхности металла атоме водорода с образованием молекулярного водорода, который десорбируется. Следовательно, реакция Гейровского, как и реакция Фольмера, является реакцией перехода. [19]
Раньше считали, что катодное выделение водорода протекает по маршруту I в виде последовательности стадий разряда и рекомбинации. Физической основой этой теории служит тот факт, что процесс рекомбинации двух атомов протекает не мгновенно ( при каждом столкновении), а с некоторой небольшой скоростью. Это вызвано выделением значительной энергии при взаимодействии двух атомов; эта энергия концентрируется в образующейся молекуле и вызывает ее обратный распад на атомы. На различных катализаторах, в частности, на металлах, реакция ускоряется за счет отвода части избыточной энергии поверхностью катализатора. [20]
Фрумкиньш применительно к процессу катодного выделения водорода. Из формулы Фрумкина вытекает, что перенапряжение зависит не только от концентрации непосредственных участников электродной реакции, но и от природы и содержания любых веществ, в первую очередь поверхностно - активных, способных изменить величину - потенциала. [21]
 |
Средние коэффициенты активности хлористых натрия и калия в водных растворах. [22] |
С измеримой скоростью процесс катодного выделения водорода по приведенной выше реакции вблизи равновесного потенциала может идти только на платинированной платине в условиях идеальной чистоты раствора. Практически выделение водорода происходит с перенапряжением. [23]
Тем самым снижается перенапряжение катодного выделения водорода. Возникающий под влиянием механических напряжений барьерный скачок потенциала Дф активирует анодное растворение металла. В итоге ускоряются одновременно и анодный и катодный процессы растворения металла [5], а количество выделяющегося водорода возрастает. При этом возрастают как роль локального анодного растворения, так и роль возможного водородного охрупчива-ния. Вопрос о приоритете того или иного механизма должен рассматриваться отдельно в каждом конкретном случае. [24]
Рассмотрим практически важный случай катодного выделения водорода. [25]
Фрумкиным применительно к процессу катодного выделения водорода. Из формулы Фрумкина вытекает, что перенапряжение зависит не только от концентрации непосредственных участников электродной реакции, но и от природы и содержания любых веществ, в первую очередь поверхностно-активных, способных изменить величину я - потенциала. В частном случае ( i 0) она превращается в формулу Эрдей-Груза и Фоль-мера. [26]
Один из вероятных механизмов катодного выделения водорода из щелочных растворов состоит в следующем. [27]
Фрумкиным применительно к процессу катодного выделения водорода Из формулы Фрумкина вытекает, что перенапряжение зависит не только от концентрации непосредственных участников электродной реакции, но и от природы и содержания любых веществ, в первую очередь поверхностно-активных, способных изменить величину - потенциала. В частном случае ( яр. [28]
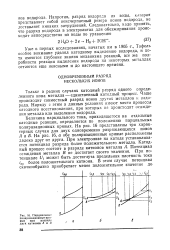 |
Парциальные поляризационные кривые при разряде двух катионов А я В. [29] |
Тафель особое внимание уделял катодному выделению водорода, и хотя имеются глубокие знания механизма реакций, все же подробности реакции выделения водорода на некоторых металлах остаются еще неясными и до настоящего времени. [30]
Страницы: 1 2 3 4