Электролитическое выделение
Cтраница 1
Электролитическое выделение этих металлов из водных растворов сопровождается очень низким перенапряжением. Так, при осаждении олова или свинца из тщательно очищенных растворов; простых солей величина перенапряжения выделения металла при i 10 ма / см. не превышает 5 - 6 мв. [1]
Электролитическое выделение некоторых щелочных и щелочноземельных металлов из их расплавленных соединений на жидком катоде из другого металла происходит значительно легче, с большим выходом по току и при меньшем напряжении, чем на твердом катоде. [2]
Электролитическое выделение в виде двуокиси часто применяется для отделения малых количеств свинца. [3]
Электролитическое выделение при заданном потенциале обеспечивает селективность определения. Точность кулонометрического анализа растет с увеличением частного от деления значения начального тока на значение остаточного тока. Мешающее влияние элетроактив-ных примесей необходимо устранять предварительным электролизом фонового электролита. Нежелательный анодный процесс можно подавить добавлением гидроксиламина, который действует как анодный деполяризатор. [4]
Электролитическое выделение Ей на ртутном катоде из растворов, содержащих ионы SO42 - [743, 1158, 1458], муравьиную или уксусную кислоту [1360], не может быть рекомендовано ввиду недостаточного выхода или неудобств, связанных с образованием осадков. При этом, кроме Yb и Sm, ни один из рзэ в амальгаму не выделяется. [5]
Электролитическое выделение может применяться для ряда элементов. При этом, к сожалению, возникают затруднения из-за неоднородности по толщине образующихся слоев и плохого прилипания осадков элементов или их окислов к материалу электрода. [6]
Электролитическое выделение молибдена, так же как н вольфрама из вотных растворов затруднено. Тонкие блестящие покрытия ыЪлиб - дена можно получить из электролита, содержащего г / л - молибдат av мония 10, плавиковую кислоту 25, осаждение проводит при 18 - 25 С и катодной плотности / к 100 А / дмЕ с нерастворимыми анодами из пла тинированного титана или графита Толщина покрытий 2 - 3 мкм. При изменении соотношения компонентов и режима электролиза в электролите могут быть почучены черные покрытия Состав электролита в этом случае, г / л: молнбдат аммония 100, плавиковая кислота 10; режим электролиза / 40 С, / к5 А / дм. [7]
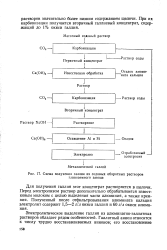 |
Схема получения галлия из содовых оборотных растворов глиноземного завода. [8] |
Электролитическое выделение галлия из алюминатно-галлатных растворов обладает рядом особенностей. [9]
Электролитическое выделение марганца возможно только благодаря высокому перенапряжению выделения водорода на этом металле. Поэтому росту выхода марганца по току способствует низкая температура, повышенное значение рН электролита и высокая катодная плотность тока. Применение высоких плотностей тока, однако, ограничено из-за ухудшения качества осадка марганца. [10]
Электролитическое выделение Pu проводят аналогично электролитическому выделению U ( см. методику выделения U, пп. [11]
Электролитическое выделение вольфрама из водных растворов связано с большими трудностями из-за его большого сродства с кислородом и низкого перенапряжения выделения водорода на вольфраме. Из водных электролитов можно получить только очень тонкие покрытия, в которых вольфрам, как правило, находится в виде оксидов. [12]
Электролитическое выделение молибдена из водных растворов, как и вольфрама, затруднено. [13]
Электролитическое выделение вольфрама и молибдена из водных растворов связано с такими же трудностями, как и осаждение металлов третьей группы периодической системы - титана, германия, циркония. Все они отличаются большой склонностью к пассивации, высоким отрицательным потенциалом, при котором возможно выделение на катоде, низким перенапряжением разряда водорода. После осаждения тонкого слоя вольфрама или молибдена преобладающую роль в процессе электролиза начинает играть выделение водорода. [14]
 |
Схема электролизера. для извлечения галлия из растворов процесса Байера. [15] |
Страницы: 1 2 3 4