Электрохимическое выделение
Cтраница 2
Методы электрохимического выделения радиоактивного изотопа для получения препаратов без носителя не могут иметь значительного распространения. Невесомая концентрация радиоактивного изотопа является причиной его медленного и неколичественного выделения. Попытка перенесения на наши случаи методов электровыделения некоторых элементов, зарекомендовавших себя в макро - или микроанализе, часто давала отрицательные результаты. Это могло происходить вследствие того, что концентрация выделяемого радиоактивного изотопа была ниже предельной, при которой возможно выделение. Это не означает, что примененный исходный раствор был слишком разбавлен. Концентрация ионов в растворе могла снизиться вследствие адсорбции ионов стенками сосуда, или образования ионами радиоколлоида, или комплексного соединения с такими ионами, которые с обычными концентрациями ионов комплексов не образуют. [16]
При электрохимическом выделении существенное значение имеет реакция среды и наличие комплексных соединений в растворе. [17]
Электролиз и электрохимическое выделение по-прежнему являются мало употребительными методами. В лаборатории НИФИ-2 [25] разрабатываются методы выделения дочернего радиоактивного изотопа из раствора соединения материнского вещества в органическом растворителе при помощи электрического поля. Такой прием также позволяет многократно использовать раствор соединения материнского изотопа для извлечения дочернего без носителя. [18]
Делали попытки электрохимического выделения железа из отработанных травильных ванн, составленных из соляной или серной кислоты. [19]
Электроды для электрохимического выделения золота изготавливают из стеклоуглерода. Процесс электролитического выделения золота ведут при напряжении 4 - 5 В, плотности тока 20 - 30 А / дм2 в течение 2 - 3 ч, расход электроэнергии - 0 2 - 0 4 кВт - ч на 1 г золота. [20]
Делали попытки электрохимического выделения железа из отработанных травильных ванн, составленных из соляной или серной кислоты. [21]
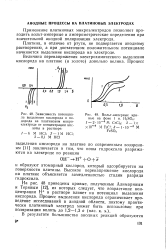 |
Зависимость потенциала выделения кислорода и водорода на платиновом микроэлектроде от концентрации кислоты в растворе.| Вольт-амперные кривые на фоне 1 н. H2SO4. - 2 - 10 - 4М СгС12. 2 - IX. [22] |
Величина перенапряжения электрохимического выделения кислорода на платине ( и золоте) довольно велика. [23]
На первый взгляд электрохимическое выделение брома кажется весьма выгодным, так как нормальный потенциал брома на 0 27 б ниже нормального потенциала хлора; следовательно, при электролизе рассола и щелоков, в которых наряду с бромистыми содержатся также и хлористые соли, ион брома будет разряжаться на аноде раньше иона хлора. [24]
На первый взгляд электрохимическое выделение брома кажется весьма выгодным, так как нормальный потенциал брома на 0 27 в ниже нормального потенциала хлора; следовательно, при электролизе рассола и щелоков, в которых наряду с бромистыми содержатся также и хлористые соли, ион брома будет разряжаться на аноде раньше иона хлора. [25]
Экспериментально подобраны условия электрохимического выделения 99 - 97 % Bi при первоначальном содержании его в ванне 1 - 10 г, в то время, как примеси з количествах 10 - 3 - 10 - 6 % оставались в растворе. [26]
Метод основан на электрохимическом выделении меди из раствора на платиновую сетку в присутствии более активного, чем медь, свинца, с которым сетка вне раствора соединена медной проволокой. [27]
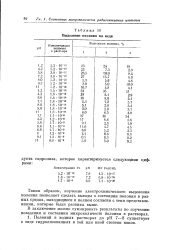 |
Выделение полония на меди. [28] |
Таким образом, изучение электрохимического выделения полония позволяет сделать выводы о состоянии полония в разных средах, находящиеся в полном согласии с теми представлениями, которые были развиты выше. [29]
Для этой цели часто используется электрохимическое выделение полония на менее благородных металлах. Так, полоний хорошо выделяется на серебре из разбавленных азотнокислых или солянокислых растворов, полностью отделяясь от свинца. [30]
Страницы: 1 2 3 4