Электрохимическое выделение
Cтраница 3
Следует отметить, что процессы электрохимического выделения сурьмы, висмута и мышьяка на катоде в виде плотных и толстых осадков изучены, главным образом, для целей гидроэлектрометаллургии. Сведения, касающиеся получения сурьмы, висмута и мышьяка в качестве покрытий [3] и механизма процесса их электроосаждения [4 - 9], немногочисленны. Особенно это относится к получению мышьяковистых покрытий, хотя и существует ряд описаний технологических процессов электроосаждения мышьяка в целях предохранения изделий от коррозии, а также для придания деталям декоративного вида. [31]
Подобные схемы предлагаются также для электрохимического выделения кислорода и анодного образования озона [24 - 33], электроокисления иодида и иода до иодата [34], сульфида и сульфита до сульфата [23, 35], урана ( IV) [36], арсенита [37], тиогликоля-та [38] и многих других неорганических и органических веществ. [32]
Блестящие осадки никеля непосредственно при электрохимическом выделении без дополнителной полировки покрытия получаются из электролитов, содержащих специальные добавки органических веществ. Некоторые из них придают электролиту также способность выравнивать микрорельеф покрытия вследствие повышения скорости осаждения никеля в микроуглублениях. Наиболее распространенными добавками в электролиты для никелирования являются 1 4-бутиндиол, хинальдин, сахарин, фталимид. Кроме того, известны эффективные электролиты, выпускаемые зарубежными фирмами, например электролиты Ni-66 ( США), содержащие в качестве основного выравнивающего агента спирты ацетиленового ряда или их производные. Обычно только сочетание двух-трех блескообразующих и выравнивающих добавок позволяет получать в достаточно широком интервале плотностей тока никелевые осадки с минимальными внутренними напряжениями. [33]
Рассмотрена роль различных факторов при электрохимическом выделении примесей на угольные электроды из растворов солей щелочных металлов. [34]
В работе [18] авторы предлагают метод электрохимического выделения щелочных ( К, Na, Li, Rb и Cs) и щелочно-зе-мельных ( Са, Ва, Sr и Mg) элементов ( 1 - 10 мкг) в виде амальгамы. Анализируемый раствор, в который добавлен раствор двухлористой ртути, подвергают электролизу при напряжении 2 5 - 3 в. При этом образуется - 500 мкг Hg, которой достаточно для связывания анализируемых металлов в амальгаму. Далее амальгаму анализируют в искре, горящей в специальной камере с откачкой. [35]
Это приводит к изменению соотношения скоростей электрохимического выделения хлора и кислорода в пользу последнего па поверхности пор, расположенных в глубине электрода. [37]
Для изучения состояния радиоактивных элементов можно применять самопроизвольное электрохимическое выделение Величина потенциала выделения зависит от концентрации свободных ионов радиоактивного изо-топа в растворе. Связывание радиоактивного изотопа в комплекс или образование гидролизован-ных ионов и коллоидных частиц вызывает сдвиг потенциала выделения. При этом количество выделенного изотопа уменьшается. Если в растворе присутствуют псевдоколлоиды, то после осаждения ионов из раствора идет постепенное разрушение псевдоколлоидов и дальнейшее выделение радиоактивного изотопа. [38]
При помощи методов адсорбции, ультрафильтрации, электрохимического выделения и др., позволяющих определять рН перехода радиоактивного изотопа в коллоидное состояние, могут быть определены величины произведений растворимости гидроокисей соответствующих элементов. Удовлетворительность совпадения полученных таким образом величин произведений растворимости для микроколичеств Ро, Zr, Nb, Ru и других элементов с величинами, полученными для макроколичеств, позволяет сделать вывод, что высказанное некоторыми исследователями предположение о невозможности достичь величины произведения растворимости в случае микроконцентраций элементов является, по-видимому, недостаточно обоснованным. [39]
Первое более или менее детальное изучение кинетики электрохимического выделения по методу Хевеши и Панета было произведено Жолио-Кюри [6], который с помощью предложенного им прибора произвел исследование процесса выделения полония на золотых электродах. [40]
При помощи методов адсорбции, ультрафильтрации, электрохимического выделения и др., позволяющих определять рН перехода радиоактивного изотопа в коллоидное состояние, могут быть определены величины произведений растворимости гидроокисей соответствующих элементов. Удовлетворительность совпадения полученных таким образом величин произведений растворимости для микроколичеств Ро, Zr, Nb, Ru и других элементов с величинами, полученными для макроколичеств, позволяет сделать вывод, что высказанное некоторыми исследователями предположение о невозможности достичь величины произведения растворимости в случае микроконцентраций элементов является, по-видимому, недостаточно обоснованным. [41]
Первое более или менее детальное изучение кинетики электрохимического выделения по методу Хевеши и Панета было произведено Жолио-Кюри [6], который с помощью предложенного им прибора произвел исследование процесса выделения полония на золотых электродах. [42]
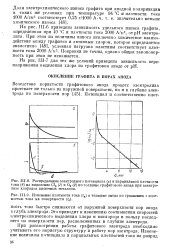
Здесь мы проводим новые данные о механизме электрохимического выделения кислорода на Ag-электроде, полученные в нашей лаборатории А. А. Яковлевой и Т. И. Борисовой различными методами. На рис. 2 представлена зависимость потенциала анодно-поляризо-ванного Ag-электрода в 1 N NaOH от логарифма s плотности поляризующего тока. На кривой рис. 2 ха - Рис-рактерны две области: при 1 55 - 1 7 б наклон кривой характеризуется величиной Ъ с 70 мв, а при 1 90 - 2 1 в - величиной - 1 60 мв; при потенциалах выше 2 0 в процесс осложняется растворением окислов серебра. Необходимо учесть, что кислород выделяется на уже окисленной поверхности серебра. Кривые 2 и 3 получены в процессе снятия кривой заряжения. [43]
Это приводит к изменению соотношений относительных скоростей электрохимического выделения хлора и кислорода. На поверхности пор, расположенных в глубине электрода, кислород выделяется с относительно большей скоростью. [44]
Сумма тока заряжения и тока, обусловленного электрохимическим выделением имеющихся примесей, называется остаточным током. [45]
Страницы: 1 2 3 4