Дифторид - кислород
Cтраница 1
Дифторид кислорода - ядовитый газ бледно-желтого цвета; термически устойчив, сильный окислитель, эффективный фторирующий агент. [1]
 |
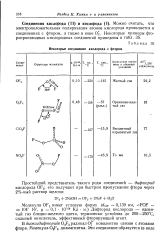
Некоторые соединения кислорода с фтором. [2] |
Дифторид кислорода - ядовитый газ бледно-желтого цвета, термически устойчив до 200 - 250 С, ( ильный окислитель, эффективный фторирующий агент. [3]
Дифторид кислорода OF2 представляет собой ядовитый газ, сгущающийся при 1 атм в жидкость при - 145 С и кристаллизующийся при - 224 С. Молекула ОР2 - угол-ковая; угол FOF равен 103, а длина OF равна 1 41 А. [4]
Дифторид кислорода очень токсичен. [5]
 |
Некоторые соединения кислорода с фтором. [6] |
Дифторид кислорода - ядовитый газ бледно-желтого цвета, термически устойчив до 200 - 250 С, сильный окислитель, эффективный фторирующий агент. [7]
Дифторид кислорода - ядовитый газ бледно-желтого цвета, термически устойчив до 200 - 250 С. [8]
Дифторид кислорода не разлагается при нагревании до температур примерно 250, но разложение более сложных окси-фторидов происходит ступенчато с образованием устойчивого OFa при очень низких температурах. Ступенчатое разложение ок-сифторидов используют для определения состава соединений. [9]
Дифторид кислорода очень токсичен. Правда, энергия активации большинства реакций с участием дифторида кислорода высока, однако ди-фторвд кислорода реагирует с некоторыми веществами со взрывом. [10]
Дифторид кислорода OF2 представляет собой ядовитый газ, сгущающийся в жидкость при 1 атм и - 145 С и кристаллизующийся при - 224 С. Молекула OF2 - уголковая; угол FOF равен 103, а длина связи О - F - 1 41 А. [11]
Дифторид кислорода в воде растворим очень слабо ( в 100 мл воды при 0 и 1 атм растворяется 4Зсл 3ОР2) [91], однако окисляющая способность OF2 по отношению к водным растворам очень велика. [12]
За исключением дифторида кислорода, вышеупомянутые ги-пофториты получаются заменой водородного атома в сильной кислоте. Вероятно, этот общий метод явится основой для успешного приготовления других гипофторитов. [13]
Химические реакции дифторида кислорода хорошо исследованы [185], однако подробное изучение большинства из них должно быть продолжено. Действительно, термическое разложение само по себе идет медленно. Величина энергии активации, полученная в результате изучения скорости реакции в интервале температур 250 - 270, составляет 41 ккал / молъ. [14]
Трифторид азота и дифторид кислорода могут оказаться в ближайшем будущем очень важными лабораторными реагентами. [15]
Страницы: 1 2 3 4