Дифторид - кислород
Cтраница 3
Смесь же водяной пар - OF2 легко детонирует, тогда как с сухим OF2 взрыва не происходит. Дифторид кислорода, как влажный, так и сухой, при умеренной температуре не действует на стекло. Кварцевое волокно в атмосфере OF2 может гореть ярким светом. Древесный уголь адсорбирует газ, после чего при нагревании может взрываться. [31]
Из них при комнатной температуре существует только OF2 - бесцветный токсичный газ с запахом фтора. Ковалентная молекула дифторида кислорода имеет структуру равнобедренного треугольника: / FOF103, a dF o0 142 нм. [32]
Кэди пишет, что запах фтористого нитроксила острый и напоминает запах дифторида кислорода. Так как при гидролизе его образуется токсичный дифторид кислорода, следует совершенно избегать его вдыхания. [33]
 |
Фрагмент диаграммы состояния системы HF-KF. [34] |
Иэвестно несколько соединений фтора с кислородом. Устойчивым при комнатной температуре является только дифторид кислорода OFj. Он образуется ( наряду с кислородом и сооном) при взаимодействии фтора с водой. [35]
Дифторид кислорода очень токсичен. Правда, энергия активации большинства реакций с участием дифторида кислорода высока, однако ди-фторвд кислорода реагирует с некоторыми веществами со взрывом. [36]
Фтористый нитроксил умеренно растворим в воде. Руфф и Квасник ш утверждают, что при реакции с водой выделяются дифторид кислорода, кислород, фтористый водород и азотная кислота. [37]
Нитрозилфторид действует на ряд элементов так же легко, как и нитро-ксилфторид, а часто даже еще легче. Характерным отличительным свойством этого соединения является способность детонировать при плавлении в присутствии жидкого дифторида кислорода. [38]
Для повышения выхода по току добавляют до 20 % фторидов щелочных металлов. Анодный газ, очищенный от фтористого водорода пропусканием над фторидом натрия, содержит дифторид кислорода, кислород и воду. Чистый дифторид кислорода получают низкотемпературной дистилляцией или методом газовой хроматографии. [39]
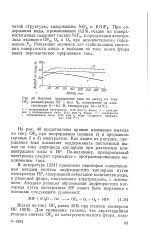 |
Влияние прерывания тока на выход по току OF2 ( концентрация KF 1 мол. %, напряжение на электролизере 6 - 6 1 В, температура 10 - 14 С. [40] |
На рис. 40 представлены кривые изменения выхода по току OF2 при непрерывном ( кривая /) и прерывном ( кривые 2 и 3) электролизе. Как видно из рисунка, прерывание тока позволяет поддерживать постоянный выход по току дифторида кислорода при различных концентрациях воды в HF. По-видимому, препаративный электролиз следует проводить с программированным выключением тока. [41]
 |
Строение некоторых полииодид-ионов. [42] |
Термодинамически OF2 более сильный окислитель, чем смесь кислорода и фтора. Молекулы OF2 имеют очень малый дипольный момент ( 0 297 Д), поэтому дифторид кислорода - одно из самых низкокипящих неорганических соединений. [43]
Формула этого вещества не подтверждена непосредственно с помощью I химического анализа, но являестя вполне вероятной. Еще один побочный продукт, которому приписывают формулу NF2, обладает j всеми свойствами загрязненного дифторида кислорода. [44]
 |
Зависимость константы скорости реакции от обратной температуры. [45] |
Страницы: 1 2 3 4