Выигрыш - энергия
Cтраница 4
Это приводит к значительно большему выигрышу энергии, чем, например, гибридизация одной s - и двух р-ор-бит с созданием трех ра-орбит в трехвалентном атоме бора. Этим в основном объясняется способность соединений трехвалентного бора присоединять вещества с неподеленными электронными парами: все связи бора при этом упрочняются благодаря переходу в тетраэдри-ческие хр3 - связи бор-аниона. [46]
Делокализация электронов сопровождается выигрышем энергии, наз. [47]
Направление процесса определится выигрышем энергии, так как уменьшение энергии стабилизирует систему. Допустим, что фактически электрон переходит от атома А к атому В. [48]
 |
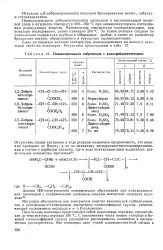
Параметры кислотной силы моделей комплексов НС1 с ИпА1С1з - п. [49] |
Отрыв протона сопровождается выигрышем энергии, т.е. в отличие от НС1 процесс является энергетически выгодным. Это подтверждается возрастанием значений заряда на атоме водорода Чн - Хотя из-за влияния d - орбиталей гертероатома хлора расчет дает заниженные значения Чн изменение ДЧн позволяет судить о росте относительной кислотной силы. Соотношение активности и селективности соответствующих катализаторов подтверждает это. Интересно, что, судя по значениям АЕ е0р и АЧн, различия в химическом строении кислот Льюиса в комплексе не проявляются и, следовательно, соответствующие анионы комплексов приблизительно равноценны. [50]
 |
Поликонденсация дибромидов с динатрийацетиленидом. [51] |
Миграция обусловлена как выигрышем энергии резонансной стабилизации, так и электронно-оттягивающим характером сложноэфирной группы, увеличивающей подвижность водорода в а - и Р - положении. [52]
 |
Схема расщепления уровня [ IMAGE ] Расщепление d - уровня в. [53] |
Достигаемый за счет этого выигрыш энергии, называемый энергией стабилизации кристаллическим полем ( ЭСКП), упрочняет химическую связь. [54]
Причиной образования связи является выигрыш энергии при образовании молекулярных орбиталей и помещении на них электронных пар. Эти пары стано вятся общими для двух атомов, между которыми возникает химическая связь. Конечно, связь может образоваться, если на связывающей орбитали будет всего один электрон. [55]
Страницы: 1 2 3 4