Выражение - константа - равновесие
Cтраница 3
Иногда применяют обратные выражения констант равновесия, представляющие собой отношение произведений концентраций исходных веществ к произведению концентраций продуктов реакции. [31]
Поставляя в выражения константы равновесия Ti 273C 500 С и Т2 700 С 273 С, находим, что К, 3 235 10 - при 500 С и К2 8 909 10 - 5 при 700 С. [32]
Поскольку в выражение константы равновесия ОВ реакции [ типа (3.9) ], наряду с активностями Ох и Red, входят также активности вспомогательных веществ А и В ( ионы водорода, гид-роксила и др.), то, изменяя их концентрацию, можно существенно сместить ОВ равновесие в нужном направлении. [33]
Такая форма выражения константы равновесия указывает, что при заданной температуре концентрация газообразного диоксида углерода над известняком и негашеной известью представляет собой постоянную величину. Сказанное верно лишь в том случае, если в наличии имеются оба твердых вещества. [34]
В результате, выражение константы равновесия может быть соответственно упрощено. [35]
Все указанные способы выражения констант равновесия применимы как для систем, находящихся при постоянных давлении и температуре, так и для систем, находящихся при постоянных объеме и температуре. [36]
Приведенный кинетический вывод выражения константы равновесия, очевидно, корректен только для элементарных реакций: константа равновесия - это отношение произведений концентраций продуктов реакции и исходных веществ в степенях, равных стехиометрическим коэффициентам в равновесной смеси. Однако на самом деле в той же формулировке он справедлив для любых реакций. [37]
Все указанные способы выражения констант равновесия применимы как для систем, находящихся при постоянных давлении и температуре, так и для систем, находящихся при постоянных объеме и температуре. [38]
Существуют два способа выражения константы равновесия: точное выражение ( так называемое термодинамическое выражение) и приближенное выражение, справедливое лишь в очень ограниченных условиях. Тем не менее приближенные константы находят широкое применение, несмотря на возможность возникновения ошибки, поскольку пользоваться ими гораздо проще. [39]
Парциальные давления в выражении константы равновесия должны быть выражены в атмосферах. [40]
В табл. VI-7 даны выражения констант равновесия для нескольких типов реакций в газовой фазе. Использование этой таблицы помогает-быстро проводить расчеты, подобные рассмотренным в примере VI-21. При определении степени превращения а по известной константе равновесия КР необходимо решить уравнение их связи, что иногда требует большого труда и времени. [41]
Концентрации, входящие в выражение константы равновесия, называются равновесными концентрация ми. [42]
В табл. 12 приведены выражения констант равновесия для некоторых других суммарных реакций. Обратите внимание, что эти выражения можно написать просто на основе уравнений суммарных реакций. [43]
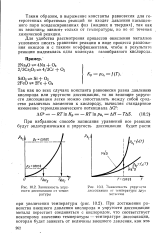 |
Зависимость упругости диссоциации от температуры.| Зависимость упругости. [44] |
Таким образом, в выражение константы равновесия для гетерогенных обратимых реакций не входят давления насыщенного пара конденсированных фаз ( жидких и твердых), так как их величины зависят только от температуры, но не от течения химической реакции. [45]
Страницы: 1 2 3 4