Квантовомеханическое выражение
Cтраница 1
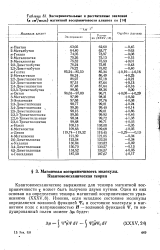 |
Экспериментальные я рассчитанные значений ( в смэ / моль магнитной восприимчивости алканоз по. [1] |
Квантовомеханическое выражение для тензора магнитной восприимчивости х может быть получено двумя путями. [2]
Используя известное квантовомеханическое выражение для энергии взаимодействия Нг и применив его с некоторыми изменениями к соединению Lla, авторы вычислили потенциалы взаимодействия атомов Li и 1Л и с помощью этих потенциалов рассчитали второй ви-риальный коэффициент. [3]
Воспользовавшись квантовомеханическими выражениями для величины момента импульса М1 и его проекции на ось квантования Мг, показать, что: а) направление момента Мг не может совпадать с выделенным в пространстве направлением; б) в пределе больших азимутальных чисел ф1 квантовый момент импульса приобретает свойства классического момента. [4]
В квантовомеханическом выражении энергии E [ v ] ( XXXI, 112) число ( XXXI, 121) также обычно обозначают через ( ок и называют волновым числом, хотя никаких колебаний, для которых сок было бы волновым числом в квантовомеханическом описании колебательных состояний молекулы, нет. [5]
Приняв в квантовомеханическом выражении для потерь энергии h i) 2Z эв, v вычислить величину потерь ( в Мэв / см) в воздухе при нормальных температуре и давлении, в алюминии, меди и свинце для протона и [ л-мезона с кинетическими энергиями 10, 100 и 1000 Мэв. [6]
Основываясь на квантовомеханическом выражении для поляризуемости атомов и постоянной вандервалльсовского взаимодействия и используя собственные волновые функции модельного гамильтониона, авторы теоретически вычислили упоклнутые величины для щелочных и щелочноземельных атомов и подобных им иолов. [7]
I были получены квантовомеханические выражения для расчета электронных энергий Еэ любых молекул. [8]
VIII было показано, что квантовомеханическое выражение для энергии образования молекулы из свободных атомов может быть представлено в аналогичной форме. [9]
Фактически этот же параметр входит и в квантовомеханическое выражение, отвечающее рассеянию пучков элементарных частиц с волновыми функциями в виде плоских волн. [10]
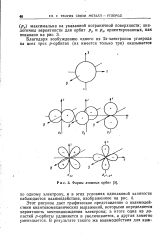 |
Формы атомных орбит. [11] |
Этот рисунок дает графическое представление о взаимодействии квантовомеханических выражений, которыми определяется вероятность местонахождения электрона; в итоге одна из лопастей р-орбиты удлиняется и увеличивается, а другая заметно уменьшается. [12]
 |
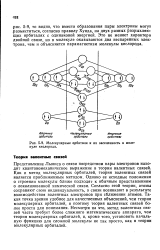
Молекулярные орбитали и их заселенность в молекуле кислорода. [13] |
Представление Льюиса о связи посредством пары электронов находит квантовомеханическое выражение в теории валентных связей. Как и метод молекулярных орбиталей, теория валентных связей является приближенным методом. Однако ее исходные положения о строении молекулы ближе подходят к обычным представлениям о локализованной химической связи. Согласно этой теории, атомы сохраняют свою индивидуальность, а связи возникают в результате взаимодействия валентных электронов при сближении атомов. [14]
 |
Молекулярные орбитали и их заселенность в молекуле кислорода. [15] |
Страницы: 1 2 3