Термодинамическое выражение
Cтраница 1
Термодинамическое выражение для произведения растворимости можно применять при расчетах растворимости только в тех случаях, когда рассматриваются очень разбавленные растворы. [1]
Термодинамическим выражением состояния вещества является его энтропия и энтальпия. Следовательно, для полимеров с высокой температурой плавления должны быть характерны или низкая энтропия плавления или высокая энтальпия - плавления. [2]
Это термодинамическое выражение, которое означает, что оно всегда справедливо. [3]
Вследствие этого термодинамическое выражение для потенциала и содержит активность ( или концентрацию) ионов в объеме раствора, вне пределов двойного слоя. Вместе с тем строение двойного слоя оказывает серьезное влияние на кинетику процесса. [4]
Вследствие этого термодинамическое выражение для потенциала и содержит активность ( или концентрацию) ионов в объеме раствора, вне пределов, двойного слоя. Вместе с тем строение двойного слоя оказывает серьезное влияние на кинетику процесса. [5]
Известно, что термодинамические выражения вполне справедливы для условий равновесия. [6]
Мембранный потенциал есть термодинамическое выражение того факта, что при равновесии мембрана, изображенная на рис. 61, должна быть поляризована, чтобы нейтрализовать градиенты концентрации ионов внутри мембраны. [7]
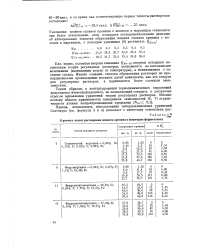 |
К расчету теплот растворения жидкого кремния в некоторых ферросплавах. [8] |
Таким образом, в конструировании термодинамических выражений допускается известный произвол, не позволяющий говорить о достаточно строгом выполнении уравнений теории регулярных растворов. [9]
Уравнение ( 4) является строгим термодинамическим выражением для химического равновесия, представленного уравнением ( 3), при условии, что величины в скобках являются термодинамическими активностями. [10]
При вычислении гж конденсирующихся компонентов используют термодинамические выражения, для упрощения которых принимают, что парциальный молярный объем компонента в жидком состоянии не зависит от давления. Для неконденсирующихся компонентов используют те же выражения, но вместо летучести чистого компонента в жидком состоянии, входящей в одно из этих выражений, применяют коэффициент Генри. [11]
Хансен и Согор [25] показали, что термодинамическое выражение, полученное Шерешевским [53] и использованное Коттоном [10], является ошибочным. [12]
Потенциал одного электрода не вхочит ни в какие термодинамические выражения для параметров, которые могут быть измерены. Поскольку имеет смысл говорить только о разностях потенциалов, одному электроду можно лроизвольно приписать нулевое значение, и все другие электроды относить к нему. Этот электрод упоминался в разд. [13]
Для нахождения количественной зависимости между АР и IR используем общее термодинамическое выражение для энергии Гельмгольца, полученное нами ранее. [14]
Полученное уравнение изменения стандартной свободной энергии является одним из наиболее полезных термодинамических выражений. [15]
Страницы: 1 2 3 4