Ион - двухвалентный кобальт
Cтраница 2
За зоной цинка следует смешанна зона, в состав которой входят ионы двухвалентного кобальта, двухвалентного никеля, двухвалентного кадмия и двухвалентного железа. [16]
Это указывает, что при данной концентрации в указанном интервале температур ионы двухвалентного кобальта практически не образуют с ионами иода сложных соединений в растворах метилового спирта. Исследование температурной зависимости светопоглощения галоидных солей кобальта в растворах метилового спирта показывает, что легкость образования кобальто-галоидных соединений при этом возрастает от кобальто-иодидных соединений к кобальто-хлоридным. [17]
По Фолку и Глэднеру, содержащая цинк карбоксипептидаза может быть активирована ионами двухвалентного кобальта в условиях, когда не происходит вытеснения одного металла другим. Допускается, что молекулы фермента находятся в растворе в двух разных конформацион-ных состояниях. Одно из них неактивно, и ионы кобальта превращают эту неактивную форму в активную. [18]
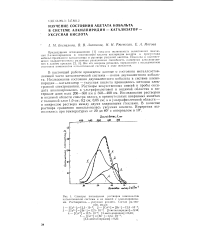 |
Спектры поглощения растворов компонентов каталитической системы и их смесей с алкилпиридина-ми. Растворитель - уксусная кислота. Состав растворов, мод / л. [19] |
В настоящей работе приведены данные о состоянии металлсостав-ляющей части каталитической системы - ионов двухвалентного кобальта. [20]
Простые ионы трехвалентного кобальта в водных растворах неустойчивы, онч легко восстанавливаются до ионов двухвалентного кобальта. [21]
Сообщается [240], что скорость растворения металлического кобальта в перекиси водорода с образованием иона двухвалентного кобальта соответствует реакции первого порядка по разности между мгновенной концентрацией кобальта в растворе и концентрацией его в состоянии насыщения и зависит от рН раствора и концентрации перекиси водорода. При более высоких рН образуется гидрат окиси трехвалентного кобальта. Наряду с этим исследование реакции кобальта с перекисью водорода [241] показало также, что растворенный ион трехвалентного кобальта количественно восстанавливается перекисью водорода. Скорость реакции соответствует первому порядку по концентрации как иона трехвалентного кобальта так и перекиси водорода и обратно пропорциональна концентрации водородных ионов. Для объяснения этого предложены две стадии с переносом одного электрона и с участием радикала пергидроксила; в реакции, возможно, как уже предложено выше для реакции с ионом четырехвалентного церия, участвуют димерпые гидратировапные ионы трехвалентного кобальта. Химия родия и иридия в реакциях с перекисью водорода не исследована. [22]
Согласно реакции ( 3), свободные радикалы брома могут образовываться при наличии в реакционной смеси ионов двухвалентного кобальта. [23]
Другой метод [1458] основан на измерении оптической плотности фенантролинового комплекса двухвалентного железа, образующегося при восстановлении комплекса трехвалентного железа ионами двухвалентного кобальта. [24]
Когда разделение ионов по длине колонки будет вполне ясным ( верхний слой бурый от трехвалентных ионов железа, средний - голубой от ионов меди, нижний бледно-фиолетовый, содержащий наиболее слабо адсорбирующиеся ионы двухвалентного кобальта), фильтрацию прекратить. [25]
Кобальт осаждают гидроокисями никеля и марганца с одновременным окислением до трехвалентного состояния. Для отделения кобальта от больших количеств никеля рекомендуется [303] осаждать ионы двухвалентного кобальта при помощи гидрозакиси никеля, а затем окислять кобальт до высшей сте пени окисления перманганатом. [26]
Ионы двух - и трехвалентного железа также образуют комплексы с 1 10-фенантролином, причем oknc - лительный потенциал этой системы несколько выше 1 в. Таким образом, в слабокислых растворах, содержащих фенантролин, ионы двухвалентного кобальта могут быть окислены до трехвалентного состояния растворами солей трехвалентного железа. [27]
Исследованы кинетические закономерности этого процесса. Отмечено наличие явления ингибировання, которое, по-видимому, связано с выводом из каталитической системы ионов двухвалентного кобальта в виде устойчивых комплексных соединений его с продуктами реакции. [28]
ЯГР такого атома 57mFe должно появиться квадрупольное расщепление, которое действительно и наблюдается. Химический сдвиг спектров 2 отвечает трехвалентному железу, и на первый взгляд кажется странным, что из ионов двухвалентного кобальта после электронного захвата в 57Со образуются ионы 57трез) хотя, казалось бы, должны образовываться ионы двухвалентного железа. [29]
Страницы: 1 2 3
