Ион - металл - переменная валентность
Cтраница 2
В технологии водоочистки в качестве катализаторов используют ионы металлов переменной валентности, такие, как Со, Ni, Си, Fe, Zn, Mn, а также различные активированные угли. Высокая окислительная способность растворов активного хлора наблюдается в присутствии марганца, который по сравнению с другими металлами способен изменять свою валентность на 4 и 5 единиц ( от 2 до 7), оставаясь устойчивым в водном растворе. [16]
 |
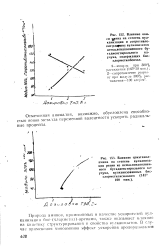
Влияние катионов некоторых металлов на выход З - хлор-2 - гидроксипропановой и щавелевой кислот. [17] |
Таким образом, присутствие в реакционной массе ионов металлов переменной валентности нежелательно. Однако учитывая очень низкую скорость коррозии титана, применение титанового оборудования в производстве ( 3 - ХМК возможно. [18]
Отмеченная аномалия, возможно, обусловлена способностью ионов металла переменной валентности ускорять радикальные процессы. [20]
Наличие магнетизма во многих окисных полупроводниках, содержащих ионы металлов переменной валентности, указывает на невозможность существования обычных энергетических зон. [21]
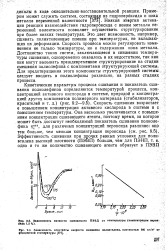 |
Зависимость вязкости сшиваемого ПЭВД от температуры ( концентрация перок.| Зависимость константы скорости сшивания полиэтилена, плотностью 960 кг / м3 от Абсолютной температуры [ 874,. [22] |
Низкая эйергия активации реакции взаимодействия гидропербксида с ионом металла переменной валентности позволяет осуществить структурирование при более низких температурах. Это дает возможность, например, сшивать полиэтиленовые пленки при температурах, не вызывающих их деформации. [23]
В проблеме стабилизации каучуков важное место занимает связывание ионов металлов переменной валентности, участвующих в окислительно-восстановительных реакциях. [24]
Метод измерений окислительных потенциалов является перспективным для изучения комплексообразования ионов металлов переменной валентности. [25]
По мнению Леви [3037, 3038], облучение способствует окислительно-восстановительным реакциям ионов металлов переменной валентности, часто вызывая окрашивание стекол. [26]
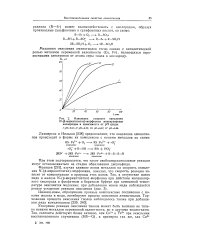 |
Изменение скорости окисления. [27] |
Ускорение реакции окисления тиолов может быть вызвано не только ионами металлов переменной валентности, но и другими веществами. [28]
Многочисленные примеры катализа стадии инициирования и стадии продолжения цепи ионами металлов переменной валентности были обнаружены при изучении окисления органических веществ. В тех случаях, когда катализаторами инициирования и продолжения цепи служат разные вещества, наблюдается эффект каталитического синергизма - скорость реакции в присутствии двух катализаторов существенно превышает сумму скоростей процессов в присутствии лишь одного катализатора. Природа этого эффекта достаточно очевидна. Катализ продолжения цепи приводит к эффективному увеличению длины цепи: v1 W / Wj W / Wj. Поскольку скорость цепной реакции определяет произведение Wt, каталитическое ускорение обеих стадий приводит к неаддитивности действия двух катализаторов. [29]
Наиболее устойчивые редокс-иониты получаются при образовании комплексов гидразина с ионами металла переменной валентности. Многие из ионов этих металлов ( Си, Cr, Mn, Fe) катализируют окисление гидразина. [30]
Страницы: 1 2 3 4