Ион - щелочной металл
Cтраница 1
 |
Коэффициенты распределения D ионов щелочных и щелочноземельных металлов на фосфате циркония ( Н - форма. [1] |
Ионы щелочных металлов не сорбируются на анионообменниках за исключением указанных ниже случаев. [2]
Ионы щелочных металлов имеют устойчивую структуру соответствующих инертных газов и очень высокий потенциал возбуждения. Спектры щелочных металлов почти такие же простые, как спектр водорода. Но по другим характеристикам водород резко отличается от щелочных металлов, хотя его единственный электрон также расположен на s - уровне. Дело в том, что в первой оболочке нет р-уровня и ближайшим разрешенным для водорода уровнем является 2р, который находится очень высоко. Наиболее интенсивная линия водорода расположена поэтому в вакуумном ультрафиолете ( К 1215 7 А) и имеет потенциал возбуждения более 10 эв. Обычно используют линии, соответствующие переходам между верхними возбужденными уровнями. Наиболее яркая линия водорода в видимой области ( К 6562 8 А) соответствует переходу 3rf - 2р и имеет потенциал возбуждения 12 1 эв. [3]
Ион щелочного металла при колебании подвергается действию сил от различных компонент раствора. Отдельно эти силы нельзя определить по единственной колебательной частоте. Эта суммарная силовая постоянная является существенным параметром, характеризующим колебание, поскольку представляет потенциальную энергию системы. Более того, она непосредственно связана с близкодействующими силами в электролитических растворах, которые так трудно оценить по термодинамическим и кондуктометрическим данным. [4]
 |
Структура краун-эфиров и криптатов. [5] |
Ионы щелочных металлов являются очень слабыми кислотами Льюиса, и значение р / Са не уменьшается даже при координации молекулы воды ( гл. Однако в последние 10 лет удалось получить поли-дентатиые лиганды, легко координируемые ионами щелочных металлов. Одним из таких лигандов являются краун-эфиры. Простые эфиры являются слабыми основаниями Льюиса, и комплексы с ионами Na и К, содержащие монодентатные лиманды с координированным эфирным кислородом, нестабильны. Однако при образовании цикла возникает структура с пяти-и шестичленными хелатными кольцами, которые сильнее связывают ионы щелочных металлов. В табл. 5.6 приведены данные о стабильности, энтальпии АЯ и энтропии образования AS0 комплексов между типичным краун-эфиром - 18-кра-ун - 6 ( рис. 5.4, а) и ионами различных непереходных элементов. [6]
Ионы щелочных металлов не восстанавливаются ни одним из восстановителей и могут быть восстановлены только электролизом. [7]
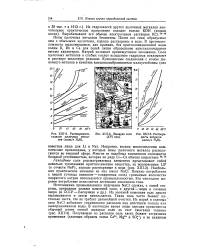 |
Растворимость галидов щелочных металлов - ( моль / л Н2О.| Выварка соли ( XVI век.| Растворимость нитратов ( моль / л Н20. [8] |
Ионы щелочных металлов бесцветны. Почти все соли, образуемые ими с обычными кислотами хорошо растворимы в воде. В противоположность выделяющимся, как правило, без кристаллизационной воды солям К, Rb и Cs для солей лития образование кристаллогидратов весьма характерно. Натрий занимает промежуточное положение. Соли щелочных металлов и слабых кислот вследствие гидролиза показывают в растворе щелочную реакцию. [9]
Ионы щелочных металлов бесцветны. Почти все соли, образуемые ими с обычными кислотами, хорошо растворимы в воде. [10]
 |
Структурные мотивы некоторых молибдатов и вольфраматов двухвалентных металлов с соотношением до. пм. [11] |
Ионы щелочных металлов стабилизируют тетраэдрическую координацию молибдена и в молибдатах некоторых переходных металлов. Подобно р-модификациям Fe [ Mo04 ] и Со [ Мо04 ], соединения состава Li2Fe2 [ Mo04 ] 8 [145] и NaCo2 31 [ Mo04 ] 3 [146] содержат тетраэдры [ Мо0412 - и шестикоор-динационные полиэдры атомов А1 и В11 ( частично В111 во втором соединении), использующие кислородные вершины молибдатных тетраэдров. В структуре Na2Co6Mo4Q40le [ 2661 атомы хлора не имеют непосредственных контактов с молибденом; поэтому структуру уместно рассматривать в разделе кислородных соединений молибдена. Координация последнего здесь тоже тетраэдрическая. [12]
Ионы щелочных металлов не способны восстанавливаться ни одним из известных восстановителей и могут быть восстановлены только путем электролиза. [13]
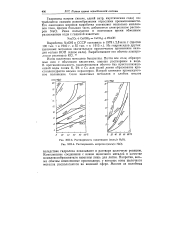 |
Растворимость галогенидов ( моль / л Н2О. [ IMAGE ] - 4. Растворимость нитратов ( моль / л ШО. [14] |
Ионы щелочных металлов бесцветны. Почти все соли, образуемые ими с обычными кислотами, хорошо растворимы в воде. В противоположность выделяющимся обычно без кристаллизационной воды солям К, Rb и Cs для солей лития образование кристаллогидратов весьма характерно. Натрий занимает промежуточное положение. [15]
Страницы: 1 2 3 4