Ион - щелочной металл
Cтраница 2
Ионы щелочных металлов ( Na, К Ь Натрий распределен в основном снаружи, а калий - внутри клетки. [16]
Ионы щелочных металлов ( Na, К 1) - Натрий распределен в основном снаружи, а калий - внутри клетки. [17]
 |
Структура краун-эфиров и криптатов. [18] |
Ионы щелочных металлов являются очень слабыми кислотами Льюиса, и значение р / Са не уменьшается даже при координации молекулы воды ( гл. Однако в последние 10 лет удалось получить поли-дентатиые лиганды, легко координируемые ионами щелочных металлов. Одним из таких лигандов являются краун-эфиры. Простые эфиры являются слабыми основаниями Льюиса, и комплексы с ионами Na и К, содержащие монодентатные лиманды с координированным эфирным кислородом, нестабильны. Однако при образовании цикла возникает структура с пяти-и шестичленными хелатными кольцами, которые сильнее связывают ионы щелочных металлов. В табл. 5.6 приведены данные о стабильности, энтальпии АЯ и энтропии образования AS0 комплексов между типичным краун-эфиром - 18-кра-ун - 6 ( рис. 5.4, а) и ионами различных непереходных элементов. [19]
Ионы щелочных металлов обладают электронной конфигурацией инертных газов, характеризующейся сферической симметрией и малой деформируемостью. Многие свойства этих ионов и их соединений находятся в связи с их ионными радиусами. [20]
Ионы щелочных металлов имеют устойчивую структуру соответствующих инертных газов и очень высокий потенциал возбуждения. Спектры щелочных металлов почти такие же простые, как спектр водорода. Но по другим характеристикам водород резко отличается от щелочных металлов, хотя его единственный электрон также расположен на s - уровне. Дело в том, что в первой оболочке нет р-уров-ня и ближайшим разрешенным для водорода уровнем является 2р, который находится очень высоко. [21]
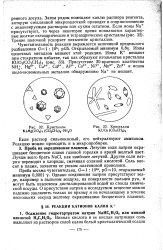 |
Кристаллы NaMg ( UOg s ( СО2СН2 9 - 9Н20. [22] |
Ионы щелочных металлов мешают этой реакции. Присутствие 20-кратного количества NH4, Hga, Cu2, Cd2, А13, Co2, Ni2, Mn2 Zn2 и ионов щелочноземельных металлов обнаружению Na не мешает. [23]
Ионы щелочных металлов отличаются от атомов инертных газов лишь наличием однократного положительного заряда. [24]
Ионы щелочных металлов бесцветны. Почти все соли, образуемые ими с обычными кислотами, хорошо растворимы в воде. В противоположность выделяющимся обычно без кристаллизационной воды солям К, Rb и Cs для солей лития весьма характерно образование кристаллогидратов Натрий занимает промежуточное положение. Соли щелочных металлов и слабых кислот вследствие гидролиза показывают в растворе щелочную реакцию. Комплексные соединения с ионом щелочного металла в качестве ком-плексообразователя известны лишь для лития. Напротив, весьма обычны комплексные производные, у которых ионы щелочного металла располагаются во внешней сфере. [25]
 |
Устойчивость триполифосфатных комплексов кальция в 1 6 % - ных растворах при различных температурах. [26] |
Ионы щелочных металлов не образуют комплексов с ортофос-фат-анионом, тогда как комплексы с полифосфат-анионами образуются и изучены. [27]
Ионы щелочных металлов не восстанавливаются под действием известных восстановителей и могут быть восстановлены только при действии электрического тока. Щелочноземельные металлы также - сильные восстановители. Они восстанавливают ион водорода из воды и кислоты. Ионы же щелочноземельных металлов можно восстановить только электролитически. [28]
 |
Элементарные ячейки в структурах LiNb6O15F ( а и NaNbsO15F ( б. [29] |
Ионы щелочных металлов опущены. [30]
Страницы: 1 2 3 4