Катодный выход - металл
Cтраница 1
Катодный выход металла по току в сульфаминовом электролите составляет - 50 % и незначительно возрастает с повышением концентрации палладия в электролите. Содержание сульфаминовокислого аммония почти не влияет на выход палладия по току. [2]
 |
Показатели качества очищенной воды при применении технологической схемы с электрохимическим корректированием рН. [3] |
Катодный выход металлов по току, как правило, небольшой. [4]
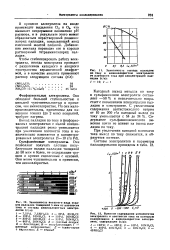
Катодный выход металлов по току резко снижается [30] с увеличением плотности тока ( фиг. [5]
С повышением температуры катодный выход металла по току возрастает. [6]
В электролите 1 катодный выход металла по току 80 - 95 %, что значительно выше, чем в цианидных растворах. Анодный выход металла по току несколько выше катодного, и поэтому электролиз ведут с применением одновременно растворимых индиевых и нерастворимых платиновых или графитовых анодов при соответствующем, подобранном экспериментально соотношении поверхностей. Получаемые покрытия толщиной до 10 мкм имеют хорошее сцепление с медью, латунью и сталью. Электролит 2 приготавливают растворением при нагревании металлического индия в разбавленной серной кислоте ( 1: 1), после чего добавляют слегка подщелоченный раствор трилона Б и сульфат аммония. [7]
 |
Циклическая вольтампер. [8] |
В тех случаях, когда катодный выход металла меньше единицы ( электроотрицательные металлы, высокие плотности тока), возникают осложнения, связанные с изменением ( обычно повышением) рН прикатодного слоя вследствие выделения водорода. Подщелачивание раствора вблизи катода благоприятствует процессам гидролиза солей металла с образованием его основных солей и гидроксвдов, которые могут влиять на ход электроосаждения и включаться в катодный осадок. [9]
 |
Циклическая вольтампер-ная кривая, полученная на Ag-элект-роде в 2 - Ю-4 М T1NO3 на фоне 0 5 М Na2SO4. скорость развертки 20 - Ю-3 В-с - 1. [10] |
В тех случаях, когда катодный выход металла меньше единицы ( электроотрицательные металлы, высокие плотности тока), возникают осложнения, связанные с изменением ( обычно повышением) рН прикатодного слоя вследствие выделения водорода. Подщелачивание раствора вблизи катода благоприятствует процессам гидролиза солей металла с образованием его основных солей и гидроксидов, которые могут влиять на ход электроосаждения и включаться в катодный осадок. [11]
В тех случаях, когда катодный выход металла меньше единицы ( электроотрицательные металлы, высокие плотности тока), возникают осложнения, связанные с изменением ( обычно повышением) рН прикатодного слоя, вследствие выделения водорода. Подщелачивание раствора вблизи катода благоприятствует процессам гидролиза солей металла с образованием его основных солей и гидроокисей, которые могут влиять на ход электроосаждения и включаться в катодный осадок. [12]
С увеличением концентрации в растворе NaCl возрастает катодный выход металла по току и рассеивающая способность электролита. Для приготовления электролита его компоненты растворяют в половинном количестве воды и вводят коллоид, после чего доливают воду до расчетного объема. [13]
Концентрация последней должна быть минимальной для обеспечения высокого катодного выхода металла по току, однако она должна быть достаточной, чтобы предупредить разложение электролита. [14]
Порядок определения анодного выхода металла по току аналогичен определению катодного выхода металла по току. [15]
Страницы: 1 2 3 4