Ион - нептуний
Cтраница 1
Ион нептуния ( У1) NpOa - нептунил-ион, так же как и нептуноил-ион, содержит кислород. [1]
Ион нептуния ( УП) NpOs - получается окислением нептуния ( VI) в растворе сильными окислителями ( озоном, K2S2Q8, гипохлоритом, гипобромитом и др.) только в щелочной среде. [2]
Ион нептуния ( VI) обозначается формулой NpOy, а ион нептуния ( V) - NpOj. Обе структуры определены на основании спектроскопических и кристаллоструктурных исследований соединений этого элемента. Съеблум и Хайндмен [33] изучили спектры поглощения ионов пяти - и шестивалентного нептуния в растворах хлорной кислоты. [3]
Ион нептуния ( Ш) Np3 неустойчив в растворе и быстро окисляется на воздухе сначала до Np4, а затем и до Npv. [4]
Ион нептуния ( 1У) Np4 устойчив в растворах. В хлорнокислых растворах ( 1 - 10 М) нептуний ( IV) существует, главным образом, в Ьиде Ыр4 - иона, а в соляно - и сернокислых растворах - в виде комплексных ионов. Ион Np4 может получаться также при растворении солей NpIV в воде или кислоте. [5]
Ион нептуния ( V) NpOj1 - нептуноил-ион содержит в своем составе кислород. Он является наиболее устойчивым состоянием окисления нептуния в растворе. Восстановление его до низких степеней окисления описано выше. [6]
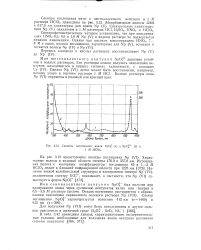 |
Спектры поглощения ионов NpO / ( 1 и NpOf (. в. [7] |
Ион семивалентного нептуния NpOi - был получен при пропускании озона через суспензию нептунатов калия или натрия в 0 5 - 3 5 М растворе щелочи. [8]
Электрохимическое поведение ионов нептуния на платиновом электроде в водных средах хорошо изучено. Показано, что сочетанием различных способов восстановления и окисления можно установить содержание ионов нептуния, присутствующих в растворе в нескольких степенях окисления. [9]
Приведенные результаты указывают на то, что ион нептуния окружен правильным октаэдром из ионов фтора и содержит один электрон в 5 / - оболочке. [10]
В табл. 2 суммированы опубликованные данные о комплек-сообразованин ионов нептуния в водных растворах. [11]
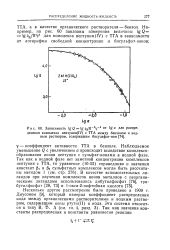 |
Зависимость lgQ lgqBar4Y - 4 от. а для РаспРе деления комплекса нептуния ( 1У с ТТА между бензолом и водным раствором, содержащим бисульфат-ион. [12] |
Наблюдаемое уменьшение Q с увеличением а происходит вследствие комплексо-образования ионов нептуния с сульфат-ионами в водной фазе. Так как в водной фазе нет заметной концентрации комплексов нептуния с ТТА, то уравнение ( 10 - 52) справедливо и значения констант PI и р2 сульфатных комплексов могли быть рассчитаны методом 1 ( см. стр. [13]
Ион нептуния ( VI) обозначается формулой NpOy, а ион нептуния ( V) - NpOj. Обе структуры определены на основании спектроскопических и кристаллоструктурных исследований соединений этого элемента. Съеблум и Хайндмен [33] изучили спектры поглощения ионов пяти - и шестивалентного нептуния в растворах хлорной кислоты. [14]
Формулы ионов плутония установлены по тому же принципу, что и формулы ионов нептуния, обозначения которых обсуждались в гл. Ион плутония ( V) обозначается формулой потому, что существует соединение плутония ( V) с формулой 2С03; кроме того, окислительно-восстановительная пара плутоний ( VI) / irayTomiE ( V) легко обратима и ее потенциал не зависит от концентрации водородных ионов. Это указывает на одинаковую степень содержания кислорода в этих ионах. [15]
Страницы: 1 2 3