Ион - перхлорат
Cтраница 1
Ионы перхлората представляют собой почти точный тетраэдр со средним расстоянием С1 - О, равным 1 42 А. [1]
Ионы перхлората с четырьмя атомами кислорода, распо - - ложенными тетраэдрически вокруг атома хлора, хорошо согласуются со структурой воды. По расчетам Форслинда [81], размер и форма такого тетраэдра приблизительно идентичны размеру и форме тетраэдра из молекул воды. Кроме того, атом кислорода иона перхлората под действием поля среды может образовать водородные связи с соседними молекулами воды без заметного искажения ее структуры. Из всех ионов, возможно, наиболее подобны воде ионы аммония: они подобны по массе, мольному объему, межатомному расстоянию, а также по величине углов - Между связями. Как было установлено в работе [26], вслед-ствие сильной полярности О - Н - связи в воде электростатическое воздействие молекулы воды на ее окружение заметно - не отличается от аналогичного воздействия иона аммония. [2]
Ионы перхлората представляют собой почти точный тетраэдр со средним расстоянием С1 - О, равным 1 42 А. [3]
Ионы перхлората со многими органическими красителями образуют ионные ассоциаты, которые хорошо экстрагируются хлороформом, бензолом, толуолом и другими органическими растворителями. Эти экстракты интенсивно ок-рашены в цвета, подобные цвету соответствующего красителя. Максимумы поглощения спектров неводных растворов ионных ассоциатов сдвинуты по сравнению с максимумами поглощения спектров водных растворов соответствующих красителей всего на 5 - 15 нм. Эти реакции используются в фотометрических методах определения многих ионов. [4]
Механизм радиолиза ионов перхлората, предложенный на основании изучения радиолитических процессов в жидких растворах, имеет тот недостаток, что ряд промежуточных стадий постулируется, как, например, образование двуокиси хлора. В жидких растворах трудно исследовать промежуточные стадии. Такие данные, в принципе, можно получать при исследовании радиолиза замороженных растворов, поскольку вторичные процессы при низких температурах существенно замедляются. [5]
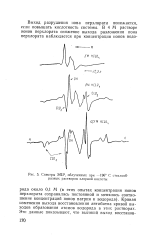 |
Спектры ЭПР, облученных при - 196 С стеклообразных растворов хлорной кислоты. [6] |
Выход разрушения иона перхлората понижается, если повышать кислотность системы. [7]
Выход разрушения иона перхлората в жидких растворах, как было показано выше, зависит от вида использованного излучения. Можно отметить, что спектр хлорнокислых растворов, облученных а-частицами, имеет такой же характер, как и для растворов, облученных у-лучаыи. [8]
Выход разложения иона перхлората при малом проценте его разрушения не зависит от дозы ни для одной соли, но при большом проценте разрушения выход падает по экспоненциальному закону [54], что согласуется с уменьшением дозы, поглощенной непосредственно ионами перхлората. [9]
Соединения, включающие ион перхлората - хлорная кислота, перхлорат аммония и другие, нашли очень широкое применение в практике, связанной с использованием ионизирующего излучения, поэтому возникает вопрос о радиационной стабильности иона перхлората в различных условиях и о механизме его радиационно-хи-мических превращений. Это заставляет обсудить достаточно обширный экспериментальный материал по радиа-ционно-химическим превращениям иона перхлората в водных растворах и в твердых солях, накопленный к настоящему времени. [10]
Выход радиационно-химического разложения иона перхлората для различных систем и условий облучения колеблется в интервале от 2 до 9 ионов на 100 эв, поглощенных ионами перхлората. Поскольку процесс его разрушения определяется в основном прямым действием излучения, величина выхода разрушения с трудом поддается управлению. [11]
Обратные процессы образования иона перхлората из продуктов его разрушения, по-видимому, энергетически невыгодны н протекают в низкой степени. [12]
Наблюдаемый выход разрушения иона перхлората пропорционален его электронной доле. При - 78 С G ( - С1ОГ) 3 8 0 3 иона на 100 эв, поглощенных ионами перхлората, что в пределах ошибки совпадает с G ( - С10Г) при комнатной температуре. При - 196 С выход прямого действия ниже, чем при комнатной температуре, и составляет 3 1 0 2 иона на 100 эв, поглощенных ионом перхлората. [13]
Кривые продуктов превращения иона перхлората в замороженных растворах нелинейны. В случае ионов хлора чем ниже температура облучения, тем меньше дозы, при которых наступает отклонение от линейности, хотя начальные выходы образования ионов хлора одинаковы при всех температурах облучения и зависят только от концентрации перхлората натрия. [14]
Вывод: возбужденные излучением ионы перхлората не распадаются с образованием ионов хлора. [15]
Страницы: 1 2 3 4