Ион - перхлорат
Cтраница 3
Для раствора хлорной кислоты, учитывая, что ионы перхлората разряжаться не могут, появление изотопа 18О в газовой фазе должно обусловливаться другими причинами. Возможно, здесь происходит изотопный обмен между адсорбированными анионами с меченым кислородом и поверхностными оксидами платины, последующий распад которых приводит к выделению кислорода, содержа щего тяжелый изотоп. Подобный же механизм не исключен и при электролизе растворов серной кислоты. [31]
Для раствора хлорной кислоты, учитывая, что ионы перхлората разряжаться не могут, появление изотопа 18О в газовой фазе должно обусловливаться другими причинами. Возможно, здесь происходит изотопный обмен между адсорбированными анионами с меченым кислородом и поверхностными оксидами платины, последующий распад которых приводит к выделению кислорода, содержащего тяжелый изотоп. Подобный же механизм не исключен и при электролизе растворов серной кислоты. [32]
Для раствора хлорной кислоты, учитывая, что ионы перхлората разряжаться не могут, появление изотопа 18О в газовой фазе должно обусловливаться другими причинами. Возможно, здесь происходит изотопный обмен между адсорбированными анионами с меченым кислородом и поверхностными окислами платины, последующий распад которых приводит к выделению кислорода, содержащего тяжелый изотоп. Подобный же механизм не исключен и при электролизе растворов серной кислоты. [33]
Подводя итоги обсуждению экспериментальных данных по радиационной химии иона перхлората в различных условиях, отметим, что ион перхлората не обладает высокой радиационно-химической стабильностью, хотя, например, это очень стойкое соединение при обычных способах химического воздействия при комнатной температуре. [34]
Ион МпС / 7 - перманганат-ион, аналогичный ионам перхлората С1О7 и периодата JO7, является сильным окислителем. [35]
Эти данные поддерживают вывод об отсутствии взаимодействия между ионом перхлората и такими радикальными продуктами радиолиза воды, как радикал ОН, НО2, О -, атом Н и гидратированный электрон. [36]
Для раствора хлорной кислоты, учитывая то, что ионы перхлората разряжаться не могут, появление изотопа 18О в газовой фазе обусловливается другими причинами. [37]
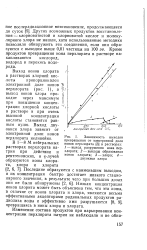 |
Зависимость выходов превращения от электронной доли ионов перхлората ( 3 ] в растворах. / - выход разрушения иона перхлората. 2 - выходы образования ионов хлората. 3 - хлора. 4 - двуокиси хлора. [38] |
Выход ионов хлората в растворах хлорной кислоты пропорционален электронной доле ионов перхлората ( рис. 1), а выход ионов хлора проходит через максимум при повышении концентрации хлорной кислоты в растворе и при очень высокой концентрации кислоты становится равным нулю. Выход двуокиси хлора зависит от электронной доли ионов перхлората нелинейно. [39]
В литературе имеются сведения только о попытке оценить константу скорости реакции иона перхлората с гидратированным электроном. Приведенное выше значение на два порядка ниже. [40]
В то же время ионы Се3 практически не изменяют выходов продуктов превращения иона перхлората. [41]
Есть и другие данные, подтверждающие отсутствие взаимодействия радикальных продуктов радиолиза воды с ионом перхлората. [42]
Обычно ошибочно предполагается, что перхлорат натрия используется в качестве ионной среды потому, что ион перхлората не дает комплексов. По крайней мере Hg ( I), Fe ( III), Ce ( III) дают перхлоратные комплексы [284], но эти вещества не могут быть идентифицированы на основании опытов в одной перхлоратной среде. JCopoino известно, что равновесные измерения не позволяют различать вещества, содержащие разные количества растворителя. [43]
Подводя итоги обсуждению экспериментальных данных по радиационной химии иона перхлората в различных условиях, отметим, что ион перхлората не обладает высокой радиационно-химической стабильностью, хотя, например, это очень стойкое соединение при обычных способах химического воздействия при комнатной температуре. [44]
Если в качестве электролита используются перхлорат тетрабутиламмония, то возникает легированный полимер, в котором на один ион перхлората приходятся три молекулы пиррола. [45]
Страницы: 1 2 3 4