Ион - платина
Cтраница 2
 |
Энергетическая диаграмма атомно-молекулярных уровней иона [ PtCl4 ] 2 -. [16] |
Часть свободных разрыхляющих орбиталей заполнена электронами, первоначально имеющимися у иона платины. [17]
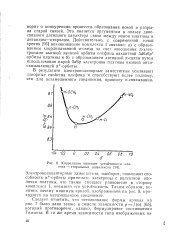 |
Корреляция констант устойчивости платина - стирольных комплексов. [18] |
Это является аргументом в пользу двое-связного дативного характера связи между ионом платины и лигандом-стиролом. Действительно, с современной точки зрения [95] возникновение комплекса I связано: а) с образованием координативной а-связи за счет заполнения л-элек-тронами высшей занятой орбиты олефина вакантной 5d6s6p9 орбиты платины и б) с образованием дативной л-связи путем использования парой 5d6p электронов платины низшей анти-связывающей я - орбиты. [19]
Плохо проводящее соединение было получено на основе других комплексов с ионами платины. В работе [813] было показано, что зеленая соль Магнуса Pf1ICli - PfI1 ( NH3) 4 состоит из одномерных платиновых цепочек с расстоянием между ионами платины 3 245 А. Замена аминогрупп на катионе затрудняет сближение молекул и предотвращает образование изоморфных материалов. [20]
При дальнейшем увеличении содержания ТБФ на бумажных полосках происходит уменьшение подвижностей исследуемых ионов платины и палладия, которые достигают минимального значения в случае бумаги, пропитанной неразбавленным раствором ТБФ. [21]
Чистая 90 % - ная Н2О2 является довольно стойким продуктом, однако, присутствие ионов платины, железа, марганца, свинца, меди ускоряет ее разложение. Скорость разложения возрастает с повышением температуры. Для повышения стойкости Н2О2 добавляют в растворы стабилизирующие вещества, например 0 5 г / л Na4P2O7 - 10H2O и 0 4 г / л салициловой кислоты. [22]
Так, при действии аммиака на хлороплатинат калия происходит не просто присоединение аммиака к иону платины ( которого в растворе практически нет), а присоединение молекул аммиака к иону платины за счет оттеснения первоначально связанных с платиной ионов хлора. Естественно, что подобного рода процессы должны протекать с большим трудом, чем процессы присоединения компонента А к свободным ионам или к ионам, относительно непрочно связанным с водой. Кроме того, очевидно, что при процессах получения гексаминов, связанных с разрушением исходных комплексных ионов, существенную роль играет прочность связи этих последних. Понятно, что надо брать такие соединения, в которых содержатся наименее прочные исходные комплексы. [23]
Так, при действии аммиака на хлороплатинат калия происходит не просто присоединение аммиака к иону платины ( которого в растворе практически нет), а присоединение молекул аммиака к иону платины за счет оттеснения первоначально связанных с платиной ионов хлора. Естественно, что подобного рода процессы должны протекать с большим трудом, чем процессы присоединения компонента А к свободным ионам или к ионам, относительно непрочно связанным с водой. Кроме того, очевидно, что при процессах получения гексаминов, связанных с разрушением исходных комплекс-дых ионов, существенную роль играет прочность связи этих последних. Понятно, что надо брать такие соединения, в которых содержатся наименее прочные исходные комплексы. [24]
Этот процесс должен идти легко, так как константа нестойкости, отвечающая присоединению первого иона циана к иону платины, на много порядков меньше, чем константа, отвечающая присоединению четвертого иона циана. Получается, что ионы [ PtCl4 ] 2 - или их аналоги должны играть роль своеобразного коллектора появляющихся в растворе ионов, более прочно связывающихся с платиной, чем хлор. [25]
 |
Орбитальная схема двойной связи в комплексе олефина с ионами Pt2. [26] |
С Н4 и двухвалентным положительным ионом Pt2 жертвуется этиленом в виде двух л-электронов двойной связи и принимается ионом платины па одну из свободных гибриди - - зованных & / 2-орбит. Это простое представление, однако, не является правильным, так как Четт и Дункенсон [5], изучавшие инфракрасные спектры, показали, что электронная структура двойных связей у этиленовых лигандов в таких соединениях почти не изменяется. Поэтому они допустили, что существует какое-то более сложное электронное взаимодействие между этиленом и ионом Pt2 [6], при котором а) свободные гибри-дизованные с. [27]
На рис. VI.19, в, и г приведены примесные спектры поглощения центров, образованных при восстановлении желатиной ионов платины и иридия. В обоих случаях в спектрах наблюдается тонкая структура. Однако структура начинает появляться лишь после 4 - 5 час. В отличие от взаимодействия желатины с солями золота, когда в конечном итоге образовывался раствор коллоидного золота, в рассматриваемых случаях восстановление не шло дальше образования атомно-молекулярных центров из соответствующих металлов. [28]
Все эти частицы выступают в качестве лигандов, конкурирующих друг с другом в координационной полусфере поверхностных комплексов платины, а ионы платины играют роль электроноакцепторных центров хемосорбции. Зто поверхностное соединение восстанавливается как целое при потенциалах первого кислородного пика катодной г, ср - кривой. [29]
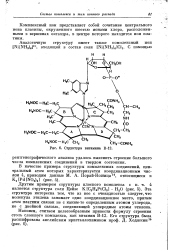 |
Структура витамина В-12. [30] |
Страницы: 1 2 3 4