Ион - радий
Cтраница 1
Ион радия Ra2 бесцветен, имеет радиус 1 37 А и электронную структуру, присущую инертным газам. [1]
Ион радия Ra2, будучи слабо гидратирован, более подвижен, чем ионы щелочноземельных металлов, и легко абсорбируется ионообменными смолами. Этим иольвуются для его отделения. [2]
Ион радия Ra2 вступает в те же микрохимические реакции, что и ион Ва2, - с гексафторокремниевой, щавелевой, винной кислотами, с цианидом аммония, ферроцианидом калия, фосфомолибдатом аммония в аммиачном растворе. [3]
Однако непосредственное экспериментальное определение радиуса иона радия рентгенографическим методом наталкивается на большие методические трудности, вследствие чего его значение не было определено до настоящего времени, Для того чтобы иметь некоторое суждение о том, насколько радиус иона радия отличается от радиуса иона бария, попробуем сравнить молярные объемы их хлористых и бромистых солей. [4]
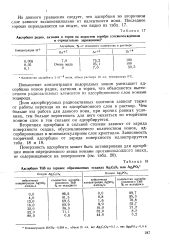 |
Адсорбция ThB на заранее образованных осадках Ag2C204 или Ag3P04. [5] |
Повышение концентрации водородных ионов уменьшает адсорбцию ионов радия, актиния и тория, что объясняется вытеснением радиоактивных элементов из адсорбционного слоя ионами водорода. [6]
Одинаковая зависимость от рН адсорбции стеклом ионов радия ( рис. 192) и одновалентного таллия ( рис. 121) позволяет полагать, что механизм адсорбции обоих ионов, по-видимому, одинаков. В этом случае не меняется характер адсорбции во всем интервале значений рН; для обоих этих элементов характерно отсутствие гидролиза их соединений. Таким образом, изменение рН среды влияет на величину адсорбции не по причине изменения формы нахождения в растворе исследуемых элементов, а в результате изменения концентрации Н - ионов, конкурирующих с ионами радия и одновалентного таллия, с одной стороны, и подавляющих диссоциацию кремнекислых групп поверхности стекла - с другой. [7]
Одинаковая зависимость от рН адсорбции стеклом ионов радия ( рис. 114) и одновалентного таллия ( рис. 59) позволяет полагать, что механизм адсорбции обоих ионов, по-видимому, одинаков. В этом случае не меняется характер адсорбции во всем интервале значений рН; для обоих этих элементов характерно отсутствие гидролиза их соединений. Таким образом, изменение рН среды влияет на величину адсорбции не по причине изменения формы нахождения в растворе исследуемых элементов, а в результате изменения концентрации Н - ионов, конкурирующих с ионами радия и одновалентного таллия, с одной стороны, и подавляющих диссоциацию кремнекислых групп поверхности стекла - с другой. [8]
Ион кальция в кристаллах может быть заменен ионами радия, стронция, бария, а гидроксильный - ионом фтора. Различают грубоволокнистую и пластинчатую костную ткань. В первой ( имеется у зародышей, а у взрослых организмов - только в области черепных швов и местах прикрепления сухожилий) волокна идут неупорядоченно, во второй ( К. [9]
С другой стороны, порядок величины коэффициента самодиффузии ионов радия в кристаллах Ва ( МОзЬ был определен в прямых диффузионных опытах методом ядер отдачи и найден равным 10 - 12 см2 / сутки. Таким образом, истинная величина этого коэффициента на 7 порядков ниже эффективного значения D, найденного из опытов по обмену. Ясно, что при установлении равновесия в отношении микрокомпонента процесс диффузии ионов радия в кристаллах бариевой соли не играет практически никакой роли, и скорость обмена определяется перекристаллизацией осадка нитрата бария. [10]
Определение удельной поверхности сернокислого свинца производится по адсорбции изоморфного иона радия. [11]
Особенно сильно адсорбируются и прочно удерживаются мелкозернистыми осадочными породами ионы радия. Радий и калий обусловливают почти всю радиоактивность глин. Породы как артинского, так и сакмар-ского горизонтов обладают низкой радиоактивностью. [12]
Присутствие избыточного количества водородных ионов защищает находящиеся при чрезвычайном разведении ионы радия от адсорбции и абсорбции его на стекле. [13]
В случае углекислых солей бария и радия вероятен морфотропный переход их структуры благодаря тому, что радиус иона радия больше радиуса иона бария. Имеются основания предполагать, что растворимости этих солей будут сильно отличаться и что в этом случае барий и радий, находясь при одинаковых концентрациях, не дадут смешанных кристаллов. [14]
Как видно из данных табл. 2.9, присутствия 0 1 мг солей висмута достаточно для предотвращения захвата кристаллами сернокислого калия ионов радия. [15]
Страницы: 1 2 3