Вычисление - растворимость
Cтраница 1
Вычисление растворимости, а также равновесных концентраций ионов в насыщенных растворах малораствсри-мых электролитов проводят на основании данных произведения растворимости так, как описано в § И и 12 ( см. стр. [1]
Вычисление растворимости, а также равновесных концентраций ионов в насыщенных растворах малорастворимых электролитов проводят на основании данных произведения растворимости так, как описаны в § 11 и 12 гл. [2]
Вычисление растворимости по известному значению ПР проводится в обратной последовательности. Найдите в вычислениях операцию, о которой часто забывают и тем самым делают ошибку в расчетах. [3]
Вычисление растворимости по известному значению ПР про водится в обратной последовательности. [4]
Вычисление растворимости с немощью этого правила совершенно аналогично определению температур кипения растворов при различных давлениях ( см. стр. [5]
Вычисление растворимости, а также равновесных концентраций ионов в насыщенных растворах малораствсри-мых электролитов проводят на основании данных произведения растворимости так, как описано в § 11 и 12 ( см. стр. [6]
Вычисление растворимости, а также равновесных концентраций ионов в насыщенных растворах малорастворимых электролитов проводят на основании данных произведения растворимости так, как описано в § 11 и 12 ( см. стр. [7]
Вычисление растворимости сульфидов в кислотах усложняется потому, что диссоциация сероводородной кислоты происходит по ступеням. [8]
Вычисление растворимости сульфидов в кислотах усложнено тем, что ионизация сероводородной кислоты происходит по ступеням. [9]
Вычисление растворимости трудно растворимых соединений, выражаемых другими формулами, проводится в том же порядке. В случае соединений, образующихся из многовалентных ионов, эти расчеты связаны с тягостными выкладками, требующими большого внимания. Принципиальных трудностей при решении задач рода не встречается. [10]
При вычислении растворимости соли в присутствии того или иного электролита необходимо учитывать коэффициенты активности его ионов. [11]
При вычислении растворимости среднерастворимых электролитов по произведению растворимости необходимо учитывать коэффициенты активности ионов. [12]
При вычислении растворимости чистого вещества в сжатом газе по закону Гиббса - Дальтона неизбежно приходится экстраполировать концентрацию пара вещества в область пересыщения. Эту экстраполяцию осуществляют по уравнению состояния вещества. Так, при вычислении растворимости эфира, хлороформа и бензола в сжатых газах экстраполяцию провели в предположении, что пары этих веществ в области пересыщения подчиняются законам идеальных газов. [13]
Рассмотрим примеры вычисления растворимости осадков в присутствии сильных электролитов. [14]
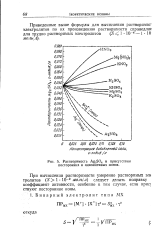 |
Растворимость Ag2S04 в присутствии посторонних и одноименных ионов. [15] |
Страницы: 1 2 3