Ион - одновалентная ртуть
Cтраница 2
Отсюда следует, что система, находящаяся в равновесии с металлической ртутью, состоит главным образом из ионов одновалентной ртути, хотя налицо имеются в заметном количестве также и ионы двухвалентной ртути. Из уравнения ( 15) следует, что константа равновесия между двумя ионами данного металла в присутствии этого же металла тем больше, чем больше разность величин стандартных потенциалов металла относительно данных ионов. Ионы, дающие более отрицательный стандартный потенциал, лри равновесии содержатся в избытке ( ср. [16]
Бели ионы двухвалентной ртути будут удаляться путем осаждения или образования комплексной соли, то должно происходить дальнейшее распадение ионов одновалентной ртути на ионы двухвалентной и металлической ртути. [17]
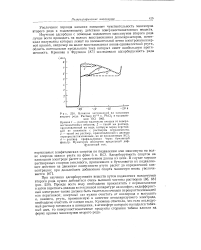 |
Влияние загрязнений на максимум второго рода. Раствор 1СГ3 н. РЬС12 в насыщенном КС1. [18] |
Изучение адсорбции с помощью подавления максимумов второго рода, лучше всего проводить на волнах восстановления деполяризаторов, потенциал полуволны которых лежит на положительной ветви электрокапиллярной кривой, например на волне восстановления ионов одновалентной ртути, область потенциалов предельного тока которых имеет наибольшую протяженность. [19]
В присутствии ионов одновалентной ртути осадок чернеет. [20]
Одновалентная ртуть при взаимодействии с дитиофосфатами дает черный осадок, нерастворимый в сильных кислотах и аммиаке. Черный цвет осадка обусловлен частичным восстановлением иона одновалентной ртути до металла. При малых концентрациях ртути вследствие уменьшения скорости реакции восстановления образуется белая муть, которая в отличие от черного осадка экстрагируется органическими растворителями. [21]
Активность иона хлора при данной температуре постоянна, вследствие наличия избытка хлористого калия. Так как и каломель имеется в избытке, то активность ионов одновалентной ртути ( определяющая потенциал электрода) остается также постоянной. Поэтому пропускание слабых токов в любом направлении не влияет на потенциал электрода. [22]
Смешивают 5 г желтой окиси ртути с 40 мл дистиллированной воды и, помешивая, постепенно добавляют 20 мл концентрированной серной кислоты. Затем добавляют новую порцию дистиллированной воды ( 40 мл) и перемешивают до полного растворения. Проверяют на наличие ионов одновалентной ртути [ Hg2 ] следующим способом. К 10 мл реактива добавляют несколько капель раствора хлористого йода, 30 мл концентрированной соляной кислоты и 20 мл дистиллированной воды. [23]
Если осадок полностью растворяется, то иона одновалентной ртути нет. Почернение осадка - есть одновалентная ртуть. [24]
В отсутствии каких-либо деполяризующих веществ ионы закиси ртути, образованные благодаря анодному растворению. Предположим, однако, что раствор содержит малую концентрацию - 0 001 М - хлор-ионов. Когда у поверхности электрода достигнута достаточно высокая концентрация ионов одновалентной ртути, превышающая произведение растворимости каломеля, каломель осаждается на поверхности электрода, и для того чтобы поддерживать концентрацию ирнов ртути на величине требуемой уравнением ( 7), должен течь больший ток. Концентрация хлор-ионов у поверхности электрода уменьшается вследствие образования каломели до величины. [25]
По этой формуле легко определить рН, измерив разность потенциалов двух спаренных водородных электродов. На практике, однако, в качестве второго электрода ( электрода сравнения) применяют не водородный нормальный насыщенный электрод, который неудобен, а так называемый нормальный насыщенный каломельный электрод, который представляет собою стеклянный сосудик той или иной формы, заполненный ртутью, каломелью и насыщенным раствором хлористого калия. Раствор хлористого калия оказывается насыщенным также и каломелью. Между ртутью и ионами одновалентной ртути в этом электроде устанавливается иная разность потенциалов, чем для нормального водородного электрода. [26]
Смесь нагреть до кипения, быстро отцентр-ифугировать и в центрифугате открыть свинец ( стр. Тщательно перемешать смесь и центрифугировать. Почернение осадка указывает на присутствие ионов одновалентной ртути. [27]
Растворы должны быть нейтральными. Молибденовый электрод в данном случае, по-видимому, функционирует как водородный электрод. Метод не имеет практического значения. Мешают хлориды и другие ионы, образующие малорастворимые соединения с ионами одновалентной ртути. [28]
 |
Полярографические волны ( вольт-амперные кривые. [29] |
Напряжение начала электролиза зависит не только от природы восстанавливающихся на катоде ионов, но и от характера анодного процесса. Напряжение разложения электролита представляет алгебраическую разность потенциалов анода и катода; оно однозначно характеризует восстанавливающиеся на катоде ионы только в том случае, если потенциал анода сохраняется неизменным. Между тем величина этого потенциала различна в зависимости от состава электролита. Стандартизация условий электролиза заключается в том, что для всех ионов указывают напряжение разложения, отнесенное к насыщенному раствору хлористого калия. Анодный процесс состоит в окислении ртути и переходе ее в раствор в виде ионов одновалентной ртути. Но в насыщенном растворе хлористого калия ионы ртути сразу образуют осадок каломели. Концентрация ионов хлора в насыщенном растворе хлористого калия остается все время постоянной, поэтому концентрация ионов ртути, а следовательно, и потенциал ртутного анода в процессе электролиза не изменяются. Если в этом случае принять потенциал анода за условный нуль, тогда напряжение начала электролиза и потенциал катода отличаются только по знаку, и на осп абсцисс графика можно откладывать вместо напряжения разложения величину Et. [30]
Страницы: 1 2 3