Ион - растворенное вещество
Cтраница 1
Ион растворенного вещества окружен сольватной оболочкой, состоящей из ориентированных дипольных молекул, прочно связанных с ионом. К этой оболочке примыкают другие молекулы растворителя, менее прочно связанные с ионом. Сильно сольватированные ионы образуют крупные сольватные комплексы, состоящие из многих слоев молекул растворителя. Поведение молекул растворителя в сольватном комплексе зависит от их расстояния от иона растворенного вещества. Молекулы, расположенные ближе всех к иону, участвуют в тепловом движении вместе с ионом Чем дальше расположена молекула растворителя от иона, тем сильнее проявляется тенденция к независимому движению. Оценка теплоты гидратации показывает, что эта теплота играет большую роль в общем энергетическом балансе растворения. [1]
Здесь ионы растворенного вещества обычно выступают в качестве акцепторов, а молекулы растворителя - в качестве доноров электронных пар. Гидраты, образующиеся в результате донорно-акцепторного взаимодействия, представляют собой частный случай комплексных соединений, рассматриваемых в главе XVIII ( аквакомплексы - см. стр. [2]
Здесь ионы растворенного вещества обычно выступают в качестве акцепторов, а молекулы растворителя - в качестве доноров электронных пар. Гидраты, образующиеся в результате донорно-акцепторного взаимодействия, представляют собой частный случай комплексных соединений, рассматриваемых в главе XVIII ( а к в а к о м п л е к с ы - см. стр. [3]
Здесь ионы растворенного вещества обычно выступают в качестве акцепторов, а молекулы растворителя - в качестве доноров электронных пар. Гидраты, образующиеся в результате донорно-акцепторного взаимодействия, представляют собой частный случай комплексных соединений, рассматриваемых в главе XVIII ( аквакомплексы - см. стр. [4]
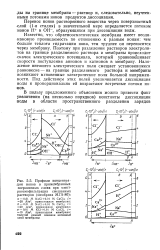 |
Профили концентрации ионов в примембранных пограничных слоях при элект-роосмофильтрации смешанных растворов ( мембрана МГА-80. [5] |
Перенос ионов растворенного вещества через поверхностный - слой ( 1-я стадия) в значительной мере определяется потоком ионов Н и ОН, образующихся при диссоциации воды. [6]
Такое взаимодействие ионов растворенного вещества друг с другом и с молекулами растворителя отражается на скорости их движения в электрическом поле, что ведет к понижению электропроводности с увеличением концентрации. [7]
Такое взаимодействие ионов растворенного вещества друг с другом и с-молекулами растворителя отражается на скорости их движения в электрическом поле, что ведет к понижению электропроводности с увеличением концентрации. [8]
Интенсивность взаимодействия ионов растворенного вещества с молекулами воды можно охарактеризовать величиной энтальпии ( теплоты) гидратации ДЯгидр - количеством теплоты, которое выделяется при переходе 1 моль ионов из вакуума в водный раствор. [9]
Интенсивность взаимодействия ионов растворенного вещества с молекулами воды может быть охарактеризована теплотой гидратации ионов А / / г - количеством теплоты, которое выделяется при переводе одного моля ионов из вакуума в водный раствор. Величина ДЯГ может быть найдена из экспериментальных данных; имеются также теоретические методы расчета. [10]
Такое взаимодействие ионов растворенного вещества друг с другом и с молекулами растворителя вызывает уменьшение скорости их движения в электрическом поле, что ведет к понижению электропроводности с увеличением концентрации. [11]
Интенсивность взаимодействия ионов растворенного вещества с молекулами воды можно охарактеризовать величиной энтальпии ( теплоты) гидратации Д - ГИДР - количеством теплоты, которое выделяется при переходе 1 моля ионов из вакуума в водный раствор. [12]
Интенсивность взаимодействия ионов растворенного вещества с молекулами воды можно охарактеризовать величиной энтальпии ( теплоты) гидратации ДЯГИДР - количеством теплоты, которое выделяется при переходе 1 моля ионов из вакуума в водный раствор. [13]
Интенсивность взаимодействия ионов растворенного вещества с молекулами воды может быть охарактеризована теплотой гидратации ионов ДЯГ - количеством теплоты, которое выделяется при переводе одного моля ионов из вакуума в водный раствор. Величина ДЯГ может быть найдена из экспериментальных данных; имеются также теоретические методы расчета. [14]
Такое взаимодействие ионов растворенного вещества друг с другом и с молекулами растворителя вызывает уменьшение скорости их движения в электрическом поле, что ведет к понижению электропроводности с увеличением концентрации. [15]
Страницы: 1 2 3 4